摘要:富含sp3杂化特征的螺环及双环结构单元作为生物电子等排体,在改善药物分子的三维性、溶解度及代谢稳定性方面具有重要价值。本文基于Spark™生物电子等排体替换工具,通过设定SMARTS筛选条件聚焦于螺环、金刚烷、立方烷及双环烷烃等富含sp3结构的片段,成功复现了两项独立研究中的分子优化过程。在MAGL抑制剂的研究中,Spark识别出能保留关键氢键相互作用的螺环替换,在五百个结果中精准筛选出作者所采用的分子。在伊马替尼的苯环替换研究中,通过收紧几何容差(距离误差小于0.25 Å,角度误差小于5°),Spark输出的2-氧杂双环[2.2.2]辛烷等替换基团能够保持与苯环相似的跨环距离及伸出矢量方向,同时显著改善化合物的ADME性质。研究表明,Spark结合SMARTS筛选与几何约束策略,能够高效发现富含sp3结构的生物电子等排体,为苗头发现与先导优化提供有力支持。
Ryan Hubball. 2026-03-20. Finding Spirocyclic and Strongly sp3 Cores as Scaffold and R-group Replacements
引言
1900年,Baeyer确立了螺环化合物的命名体系,这类化学结构单元的特征是两个环共用同一个季碳原子1。首个螺环类药物灰黄霉素(Griseofulvin)——一种抗真菌药物——于1959年获批上市2。此后,螺环结构单元在药物设计中屡见不鲜,例如CGRP受体拮抗剂Ubrogepant3、DNA促旋酶抑制剂ETX09144以及最新发现的泛冠状病毒抑制剂ASAP-00174455(图1)。
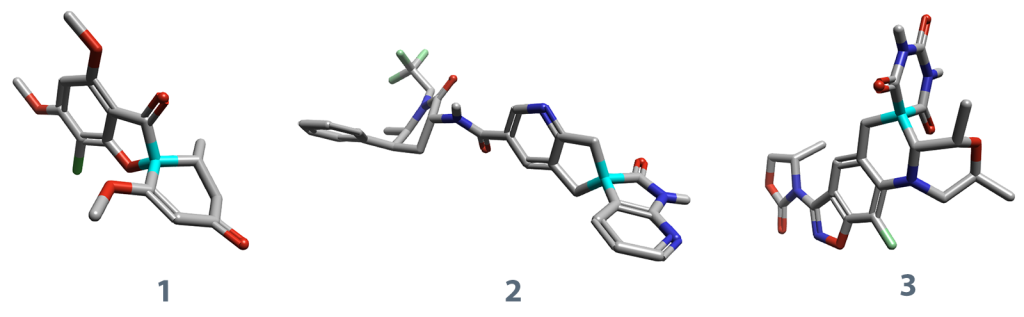
图1. Griseofulvin(1)、Ubrogepant(2)和ETX0914(3)的化学结构(采用Flare™软件呈现三维结构)。螺环季碳原子以青色标示。
因其在分子设计过程中可带来诸多益处6,近年来螺环化合物在药物研发项目中受到越来越多的关注。它们可作为常见杂环的生物电子等排体,用于调控脂溶性和pKa等性质。由于其三维立体性,螺环可通过减少晶体堆积来提高溶解度。在代谢易感位点附近引入额外的空间位阻,可以改善代谢稳定性问题7。由于螺环含有多个sp3杂化碳原子,它们能够提供新的伸出矢量(exit vectors,通常指从母核骨架向外延伸的化学键的方向或伸出矢量),从而伸向难以触及的结合口袋。基于这些特性,将螺环结构整合到化合物中不失为一条颇具潜力的设计路径。
sp3杂化碳原子分数(Fsp3)是衡量分子三维复杂性的常用指标,如前所述,提升这一指标可促进药物发现8。除了向分子中引入螺环之外,采用富含sp3结构的生物电子等排体替代苯环也是一种常用的化合物优化策略。用更具三维立体性的取代基替代这些平面环状结构,能够产生与引入螺环母核相似的益处9。在BCL‑XL抑制剂A‑133185210和自分泌运动因子抑制剂ONO‑843050611(图2)中,可以看到通过引入富含sp3的结构单元来产生新的相互作用矢量,并通过刚性化增强活性的实例。
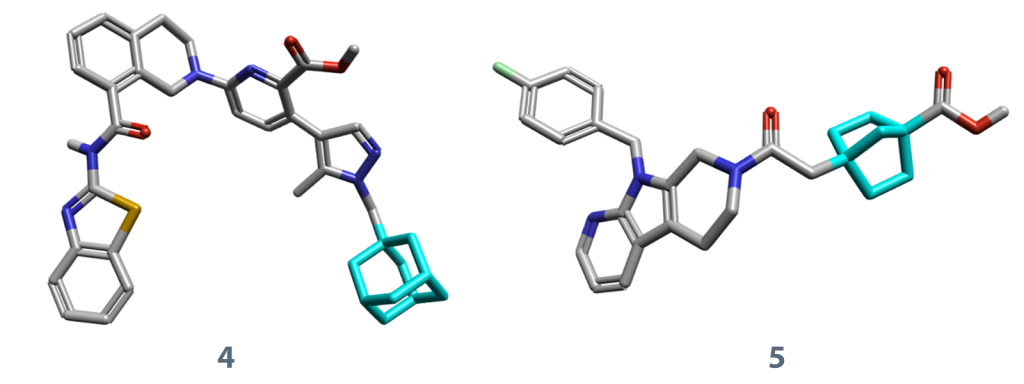
图2. A-1331852(4)引入了金刚烷基团(青色标示),与BCL-XL的关键结合口袋产生了高效的相互作用。ONO-8430506(5)引入了双环[2.2.1]庚烷结构(青色标示),使分子刚化,从而提高了其血浆活性。
Cresset公司的生物电子等排体替换工具Spark™能够推荐富含sp3结构的设计元素,从而实现上述益处。通过使用恰当的SMARTS筛选条件聚焦化合物库搜索,Spark将推荐具有高球形度且与输入分子的形状相似性及三维相似性(通过Cresset的分子场点来模拟静电、范德华力和疏水作用12)高度匹配的结构单元。
从双环到螺环:一个示例性说明
Ikeda等人致力于探究单酰甘油脂肪酶(MAGL)抑制剂的螺环衍生物如何改善化合物性质13。苗头化合物6(图3)因其双环结构单元与关键的His121和Arg57残基形成相互作用而被确定为起始点。为保留这些相互作用,研究人员迭代地替换了不同的基团,并测定了其活性及亲脂性配体效率。最终,他们引入了新颖的螺环骨架,作为3-氧代-3,4-二氢-2H-苯并[b][1,4]噁嗪-6-基结构单元的生物电子等排体。
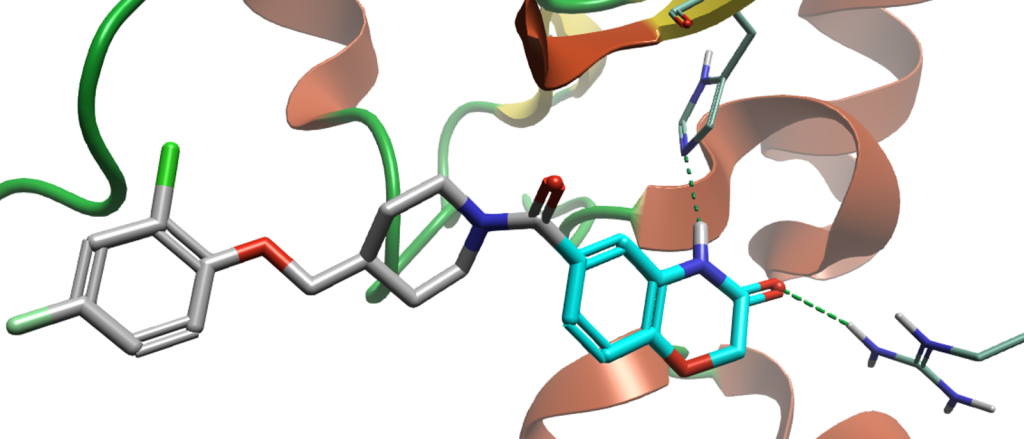
图3. Ikeda等人报道的配体(6),展示了其与His121和Arg57之间需保留的两个氢键相互作用。分子中待替换的部分以青色高亮显示。
从苯环到螺环与脂肪环:一个示例性说明
Levterov等人研究了2-氧杂双环[2.2.2]辛烷作为对位取代苯环的生物电子等排体14。苯环在天然产物和生物活性化合物中无处不在,但可能导致溶解度差等不良性质。
对2-氧杂双环[2.2.2]辛烷的晶体学分析表明,其跨环距离与伊马替尼(Imatinib)中的苯环非常相似(图4),而双环[1.1.1]戊烷等苯环生物电子等排体则存在距离不匹配的问题。2-氧杂双环[2.2.2]辛烷还能较好地保持伸出矢量的共线性,从而维持分子的整体形状。将氧原子引入双环[2.2.2]辛烷环中可提高该基团的溶解性。
当将该结构替换到伊马替尼中后,含有2-氧杂双环[2.2.2]辛烷的化合物表现出显著提高的溶解度、延长的代谢半衰期以及整体改善的ADME性质。
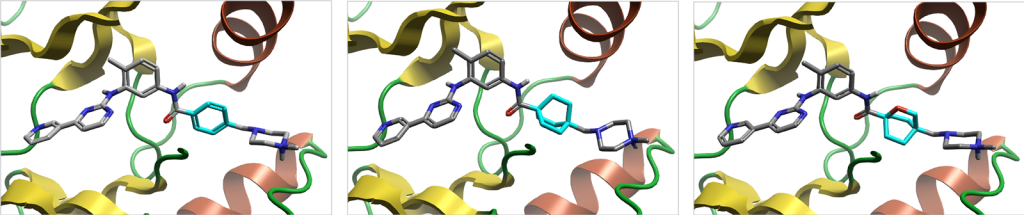
图4. 伊马替尼(7),其对位苯环以青色高亮显示。同时展示了其生物电子等排体替换后的化合物(8,9),其中的苯环生物电子等排体也以青色高亮显示。
使用Spark发现螺环候选分子
我们旨在通过进行两个独立的Spark实验来探索这些生物电子等排替换。将起始分子输入Spark,然后运行聚焦于螺环及富含sp3结构单元的搜索,我们力图找到作者所选用的替换基团以及其他有效的替代方案(图5)。
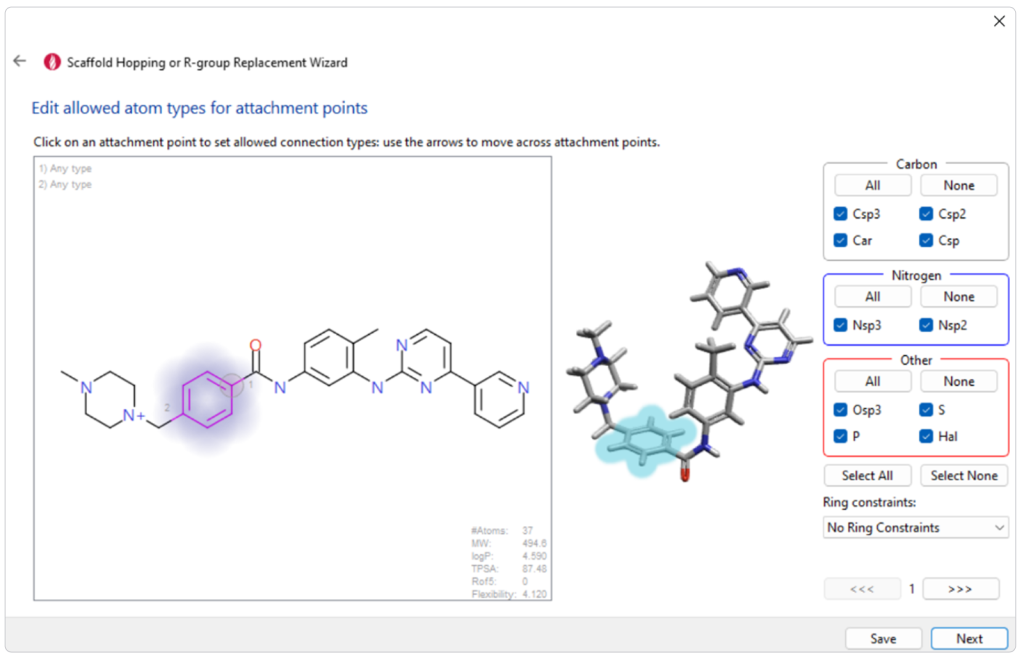
图5. Spark中输入用于替换伊马替尼中苯环的界面。分子中待替换的部分(此处为对位苯环)已被选中。在右侧菜单中,我们允许连接点的所有可能性,且未定义任何环系约束条件。
单酰甘油脂肪酶抑制剂:替换芳香环
为了复现Ikeda等人的研究搜索(他们旨在通过引入螺环结构单元来发现可逆的MAGL抑制剂),我们在采用默认Spark设置的同时,在高级筛选选项卡中引入了以下SMARTS筛选条件:
表1. 用于指示Spark仅输出符合这些模式的替换结构单元的SMARTS字符串。所使用的这些SMARTS还允许搜索结构相近的化合物。例如,表中所示的双环己烷SMARTS也会返回双环己烯、双环己酮、二氮杂双环己烷等结构。
| 组分 | SMARTS字符串 |
|---|---|
| 螺环 | [X4;R2;r](@[r])(@[r])@[r] |
| 金刚烷 | A~1~A~2~A~A~3~A~A(~A~A~1~A~3)~A~2 |
| 立方烷 | A~1~2~A~3~A~4~A~1~A~5~A~2~A~3~A~4~5 |
| 双环辛烷 | A~1~2~A~A~A(~A~A~1)~A~A~2 |
| 双环己烷 | A~1~2~A~A(~A~A~1)~A~2 |
| 双环戊烷 | A~1~2~A~A(~A~1)~A~2 |
Cresset公司的Spark能够识别出本研究中展示的生物电子等排替换,并且这些搜索无需使用自定义化合物库;富含sp3结构的片段可直接从Cresset分发的Spark默认使用的ChEMBL和SureChEMBL数据库中获得(图6)。
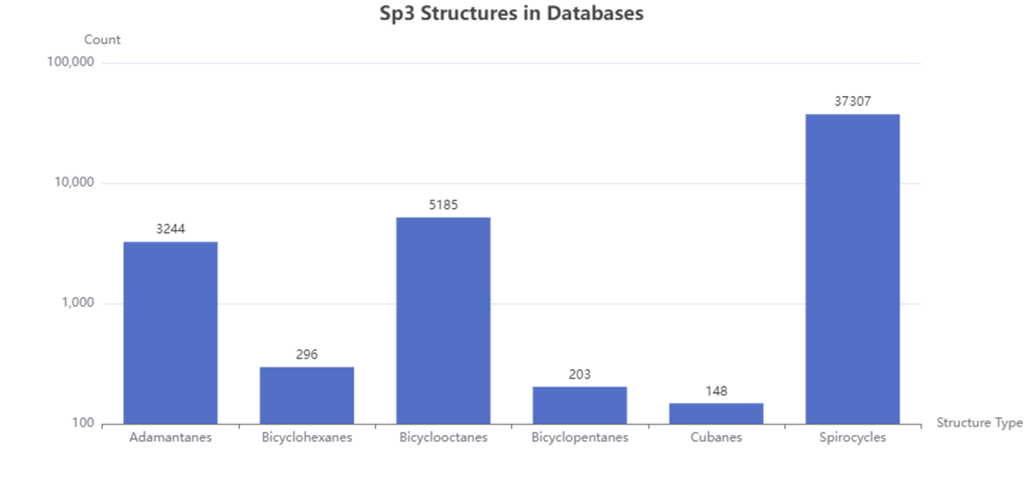
图6. 使用表1所示SMARTS字符串,在ChEMBL和SureChEMBL数据库中检出的命名子结构存在情况。
进一步的处理有助于优化Spark输出的结果。针对Ikeda等人的案例,我们对结果进行了构象搜索与叠合分析(Conf Hunt & Align)。具体操作上,我们选择了快速构象搜索(Quick Conf Hunt)和最大公共子结构叠合(MCS Alignment),并以输入分子作为参考。
Ikeda等人指出,与His121和Arg57形成的氢键对于高效结合至关重要。因此,我们利用Flare中的Python解释器脚本,为能够形成这些关键接触的结果添加标记(如需此Python脚本,请联系Cresset技术支持)。随后,这些标记可用于生成保留了这些关键相互作用的化合物列表,以便进行聚焦分析。在生成的五百个结果中,该方法识别出十二个符合条件的分子,其中包括作者合成出的那个分子(图7)。
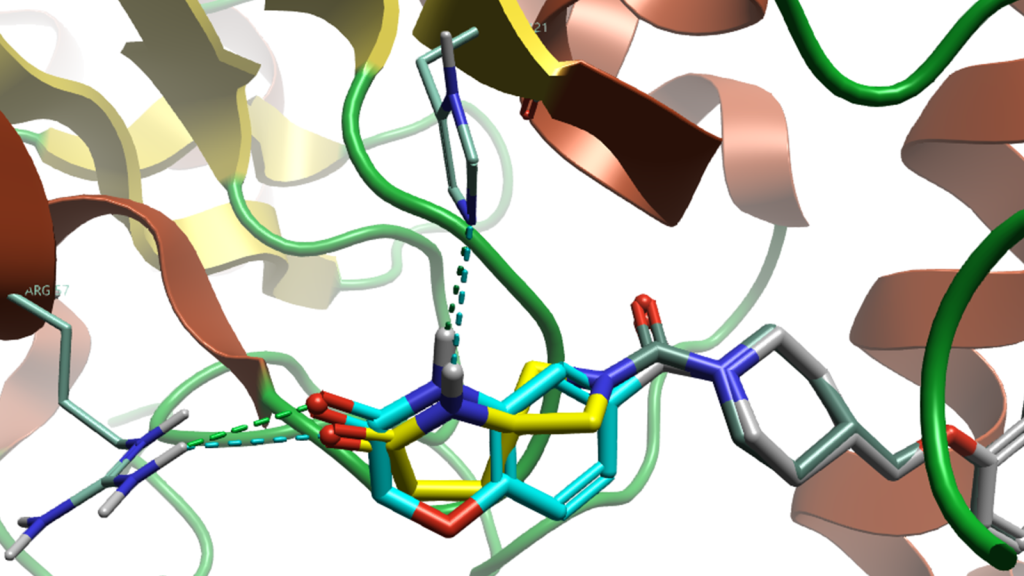
图7. 我们的输入分子(6),其中待替换的R基团以浅青色高亮显示;与Spark结果中显示的Ikeda等人的分子(10)进行叠合,后者中替换后的R基团以黄色标示。
已知药物中苯环被2-氧杂双环[2.2.2]辛烷的替换
针对Levterov等人的研究14(该研究考察了在伊马替尼和伏立诺他中用2-氧杂双环[2.2.2]辛烷母核替换苯环所产生的效应),我们在运行Spark时,除使用前述SMARTS模式外,还增加了一些额外的约束条件。该研究的一个关键要点是:与输入分子中的苯环相比,生物电子等排体替换后的跨环距离及伸出矢量方向需保持一致。因此,我们编辑了Spark的高级设置,以降低搜索的几何容差。这确保了输出分子中替换基团的伸出矢量在空间上与输入分子中苯环的伸出矢量相似。具体操作是在Spark向导的高级选项中将“允许的连接点距离误差”(Allowed attachment point distance error)和“允许的连接点角度误差”(Allowed attachment point angle error)调整为建议的最低值(图8)。
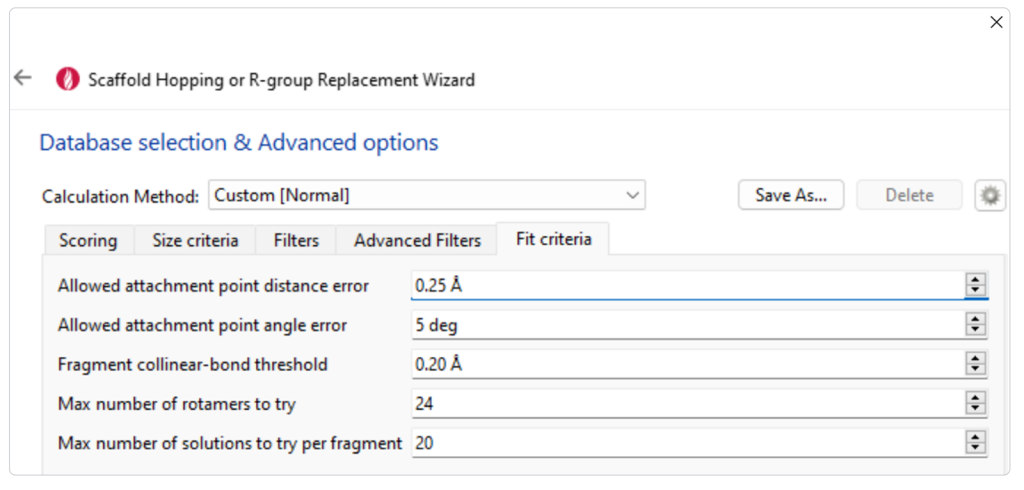
图8. Spark骨架跃迁或R基团替换向导中的高级选项。我们将“允许的连接点距离误差”调整为0.25 Å,将“允许的连接点角度误差”调整为5度。这将使Spark输出结果中替换基团的物理距离和角度与输入部分更加接近。
该实验的输出结果从ChEMBL和SureChEMBL数据库中给出了59个骨架替换建议(图9)。通过剔除那些被标记为含有不稳定结构单元的分子,我们将其筛选至51个建议。2-氧杂双环[2.2.2]辛烷和双环[2.2.2]辛烷均出现在这些结果中,并显示出正向的BIF%评分(生物电子等排体因子,用于衡量生物电子等排体替换与输入结构单元的匹配程度)。
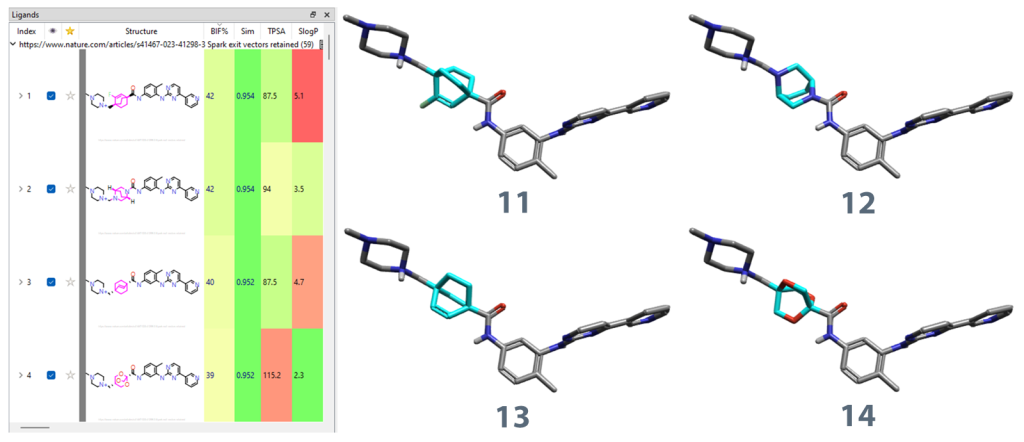
图9. Spark实验输出的前4个结果(11, 12, 13, 14)及其相关评分与指标。替换后的骨架部分以青色显示。
结论
通过利用Spark软件中提供的SMARTS筛选条件,药物化学家可以将搜索聚焦于富含sp3杂化特征的片段上,从而获得生物电子等排体设计思路。借助这类富含sp3结构环系的独特性质,可以实现具有更优性质的化合物设计。本文中,我们展示了Spark如何复现了两项旨在引入富含sp3结构单元以改善已知活性分子性质的研究结果。
通过合理使用筛选条件,Spark不仅能提供用于苗头化合物发现的思路,还能为先导化合物优化提供方案,从而改善化合物的溶解度、代谢稳定性等性质。
文献
- Baeyer, A. Systematik Und Nomenclatur Bicyclischer Kohlenwasserstoffe. Berichte der deutschen chemischen Gesellschaft 1900, 33 (3), 3771–3775. https://doi.org/10.1002/cber.190003303187.
- Martin, A. R. For the Treatment of Animals Especially, by Oral Admin Istration, the Griseofulvin May First Be Incorporated into GRISEOFULVIN USES AND COMPOSITIONS Food Premixes and the Said Premixes Then Used for Incor.
- Moore, E.; Fraley, M. E.; Bell, I. M.; Burgey, C. S.; White, R. B.; Li, C.-C.; Regan, C. P.; Danziger, A.; Michener, M. S.; Hostetler, E.; Banerjee, P.; Salvatore, C. Characterization of Ubrogepant: A Potent and Selective Antagonist of the Human Calcitonin Gene‒ Related Peptide Receptor. The Journal of Pharmacology and Experimental Therapeutics 2020, 373 (1), 160–166. https://doi.org/10.1124/jpet.119.261065.
- Basarab, G. S.; Doig, P.; Galullo, V.; Kern, G.; Kimzey, A.; Kutschke, A.; Newman, J. P.; Morningstar, M.; Mueller, J.; Otterson, L.; Vishwanathan, K.; Zhou, F.; Gowravaram, M. Discovery of Novel DNA Gyrase Inhibiting Spiropyrimidinetriones: Benzisoxazole Fusion with N-Linked Oxazolidinone Substituents Leading to a Clinical Candidate (ETX0914). J. Med. Chem. 2015, 58 (15), 6264–6282. https://doi.org/10.1021/acs.jmedchem.5b00863.
- Antiviral unveiled that goes after multiple coronaviruses. Chemical & Engineering News. https://cen.acs.org/acs-news/acs-meeting-news/Antiviral-unveiled-goes-multiple-coronaviruses/103/web/2025/03 (accessed 2025-03-31).
- Varela, M. T.; Dias, G. G.; de Oliveira, L. F. N.; de Oliveira, R. G.; Aguiar, F. D.; Nogueira, J. P.; Cruz, L. R.; Dias, L. C. Spirocyclic Compounds as Innovative Tools in Drug Discovery for Medicinal Chemists. European Journal of Medicinal Chemistry 2025, 287, 117368. https://doi.org/10.1016/j.ejmech.2025.117368.
- Griffith, D. A.; Kung, D. W.; Esler, W. P.; Amor, P. A.; Bagley, S. W.; Beysen, C.; Carvajal-Gonzalez, S.; Doran, S. D.; Limberakis, C.; Mathiowetz, A. M.; McPherson, K.; Price, D. A.; Ravussin, E.; Sonnenberg, G. E.; Southers, J. A.; Sweet, L. J.; Turner, S. M.; Vajdos, F. F. Decreasing the Rate of Metabolic Ketone Reduction in the Discovery of a Clinical Acetyl-CoA Carboxylase Inhibitor for the Treatment of Diabetes. J. Med. Chem. 2014, 57 (24), 10512–10526. https://doi.org/10.1021/jm5016022.
- Wei, W.; Cherukupalli, S.; Jing, L.; Liu, X.; Zhan, P. Fsp3: A New Parameter for Drug-Likeness. Drug Discovery Today 2020, 25 (10), 1839–1845. https://doi.org/10.1016/j.drudis.2020.07.017.
- Tsien, J.; Hu, C.; Merchant, R. R.; Qin, T. Three-Dimensional Saturated C(Sp3)-Rich Bioisosteres for Benzene. Nat Rev Chem 2024, 8 (8), 605–627. https://doi.org/10.1038/s41570-024-00623-0.
- Wang, L.; Doherty, G. A.; Judd, A. S.; Tao, Z.-F.; Hansen, T. M.; Frey, R. R.; Song, X.; Bruncko, M.; Kunzer, A. R.; Wang, X.; Wendt, M. D.; Flygare, J. A.; Catron, N. D.; Judge, R. A.; Park, C. H.; Shekhar, S.; Phillips, D. C.; Nimmer, P.; Smith, M. L.; Tahir, S. K.; Xiao, Y.; Xue, J.; Zhang, H.; Le, P. N.; Mitten, M. J.; Boghaert, E. R.; Gao, W.; Kovar, P.; Choo, E. F.; Diaz, D.; Fairbrother, W. J.; Elmore, S. W.; Sampath, D.; Leverson, J. D.; Souers, A. J. Discovery of A-1331852, a First-in-Class, Potent, and Orally-Bioavailable BCL-XL Inhibitor. ACS Med. Chem. Lett. 2020, 11 (10), 1829–1836. https://doi.org/10.1021/acsmedchemlett.9b00568.
- Iwaki, Y.; Ohhata, A.; Nakatani, S.; Hisaichi, K.; Okabe, Y.; Hiramatsu, A.; Watanabe, T.; Yamamoto, S.; Nishiyama, T.; Kobayashi, J.; Hirooka, Y.; Moriguchi, H.; Maeda, T.; Katoh, M.; Komichi, Y.; Ota, H.; Matsumura, N.; Okada, M.; Sugiyama, T.; Saga, H.; Imagawa, A. ONO-8430506: A Novel Autotaxin Inhibitor That Enhances the Antitumor Effect of Paclitaxel in a Breast Cancer Model. ACS Med. Chem. Lett. 2020, 11 (6), 1335–1341. https://doi.org/10.1021/acsmedchemlett.0c00200.
- Science overview | Cresset. https://cresset-group.com/science/overview/ (accessed 2025-07-01).
- Ikeda, S.; Sugiyama, H.; Tokuhara, H.; Murakami, M.; Nakamura, M.; Oguro, Y.; Aida, J.; Morishita, N.; Sogabe, S.; Dougan, D. R.; Gay, S. C.; Qin, L.; Arimura, N.; Takahashi, Y.; Sasaki, M.; Kamada, Y.; Aoyama, K.; Kimoto, K.; Kamata, M. Design and Synthesis of Novel Spiro Derivatives as Potent and Reversible Monoacylglycerol Lipase (MAGL) Inhibitors: Bioisosteric Transformation from 3-Oxo-3,4-Dihydro-2H-Benzo[b][1,4]Oxazin-6-Yl Moiety. J. Med. Chem. 2021, 64 (15), 11014–11044. https://doi.org/10.1021/acs.jmedchem.1c00432.
- Levterov, V. V.; Panasiuk, Y.; Sahun, K.; Stashkevych, O.; Badlo, V.; Shablykin, O.; Sadkova, I.; Bortnichuk, L.; Klymenko-Ulianov, O.; Holota, Y.; Lachmann, L.; Borysko, P.; Horbatok, K.; Bodenchuk, I.; Bas, Y.; Dudenko, D.; Mykhailiuk, P. K. 2-Oxabicyclo[2.2.2]Octane as a New Bioisostere of the Phenyl Ring. Nat Commun 2023, 14 (1), 5608. https://doi.org/10.1038/s41467-023-41298-3.



