摘要:本文探讨了理性氟扫描(Fluorine Scan)在基于结构的药物设计中的应用。通过分析罗氏团队对布鲁顿酪氨酸激酶(BTK)抑制剂的优化案例,演示了如何基于共晶结构(PDB: 4RFY)理性选择氟取代位点,使先导化合物活性提升达40倍。研究进一步表明,静电互补性(EC)打分可作为一种快速、直观的计算工具,有效定位能通过引入氟原子改善静电匹配的潜在热点。此外,结合GIST与3D-RISM水分析技术,可从水合位点与水合自由能角度评估并确认氟原子置换不利水分子的可行性。该工作展示了将Flare 场技术与水分析技术相结合的计算策略,能为理性氟扫描提供更全面、可靠的设计依据,显著提升先导化合物优化的效率与成功率。
氟扫描(Fluorine Scan,简称F-Scan)是在先导化合物优化阶段采用的一种关键药物化学策略,其核心在于系统性地用氟原子取代分子中的氢原子,以评估该取代对化合物活性、选择性及药代动力学性质的潜在影响。有效的氟扫描并非盲目进行,而是通常需要基于对蛋白-配体复合物高分辨率三维结构的仔细审视,从而理性选择那些在空间上可能通过氟取代与蛋白质环境形成特定有利相互作用的位点。在罗氏(Hoffmann-La Roche)的Lou等人1,2所开展的理性氟扫描研究中,他们明确提出了氟原子可能增强结合的四种相互作用模式:
- 氟原子与蛋白质羰基的LUMO轨道相互作用;
- 氟取代增强相邻芳香C-H键与蛋白质残基的相互作用;
- 氟原子与极性基团形成静电相互作用;
- 氟原子参与疏水相互作用。
在该研究中,基于对先导化合物与靶点蛋白(BTK)共晶结构(PDB: 4RFY)的分析,研究者识别了三个潜在的氟取代位点(文中称为向量a, b, c)。通过合成并测试系列“匹配对”化合物,他们发现其中一个位点(向量c)的氟取代能够显著提升抑制活性,特别是在不饱和双环骨架上,该位点的氟取代实现了约40倍的活性提升(如化合物6a到6b的优化,图1)。
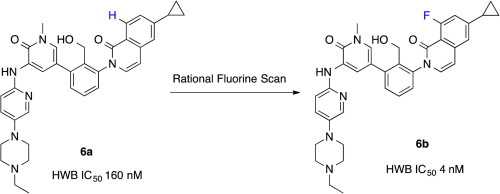
图1. 化合物6a与6b的化学结构式
尽管基于结构的可视化工具(如图2所示)能够直观展示化合物6b中异喹啉酮片段5位氟原子与蛋白质环境(如Phe413的C-H、水分子HOH807、Lys430的阳离子胺基)的空间邻近关系,但要准确解读这些近距离接触具体对应哪些类型的有利相互作用(例如,是偶极-偶极、C–H…F氢键、还是静电相互作用),仍需深厚的专业知识。对于普通药物化学研究人员而言,仅凭视觉判断难以直接、准确地进行定性,因此有必要寻求更简单、可量化的计算分析方法来辅助或部分替代此类传统的、高度依赖经验的分析方法。
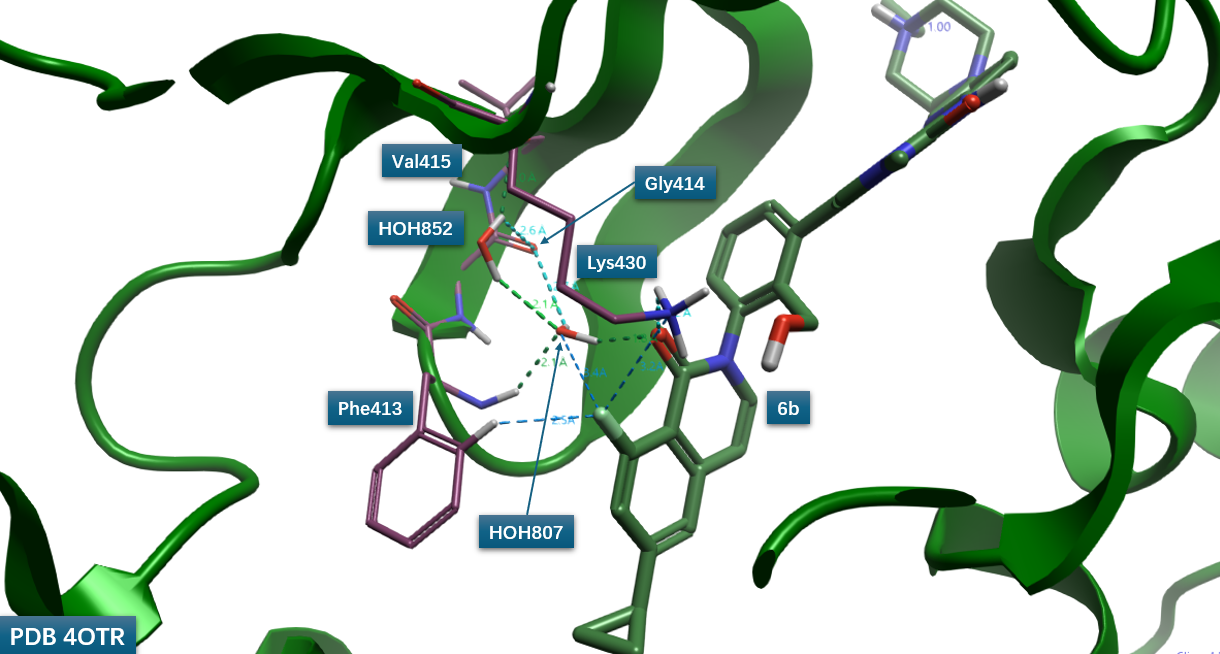
图2. 化合物6b氟原子与蛋白之间的相互作用(基于PDB 4OTR)。飘带图:BTK蛋白;绿色棍棒模型:配体6b。图片用Flare V113制作。
静电互补性打分(Electrostatic Complementarity score, EC score)是一种用于量化配体与蛋白质结合口袋之间静电势匹配程度的计算方法4。其核心原理在于:当配体表面的静电势分布与受体口袋表面的静电势分布在空间上呈互补模式(即配体的负电势区域对应蛋白的正电势区域,反之亦然)时,两者之间的静电相互作用达到最优,从而有助于提高结合亲和力。Bauer 等人4的研究表明,当一系列类似物的活性差异主要源于静电性质变化时,EC打分与实验测得的结合亲和力之间存在良好的相关性。鉴于氟扫描策略的核心在于系统比较仅有一个氟原子差异的“匹配对”化合物,其活性变化很可能与局部静电环境的改变密切相关,因此非常适合采用EC打分来理性预测和评估潜在的氟取代位点。
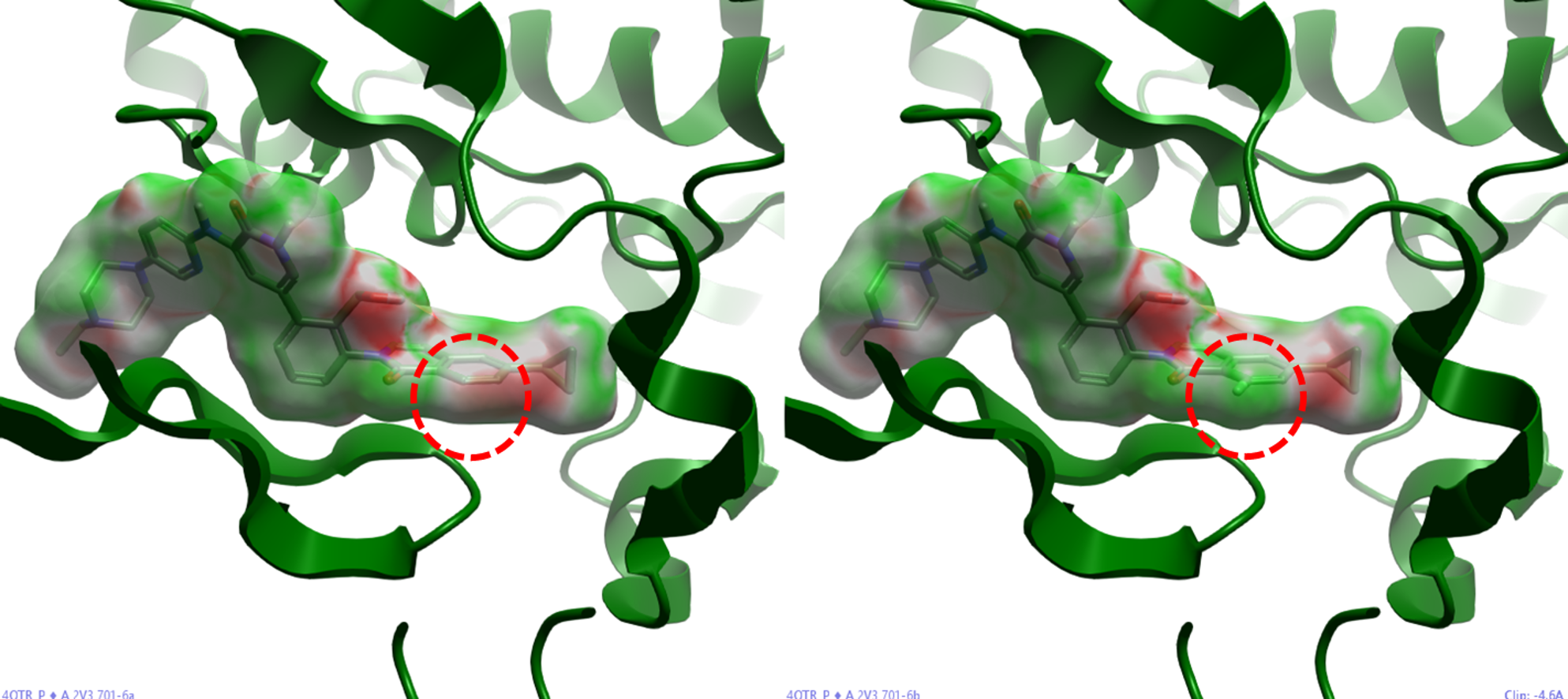
图3. 化合物6a与6b的静电互补性打分分子表面。飘带图:BTK(PDB 4TOR);分子表面-左:6a;分子表面-右;6b。分子表面按静电互补性着色,红色:不互补;绿色:互补。
以本案例中的化合物6a(未氟化)和6b(氟化)为例。在Flare软件中,对6a的分子表面进行EC打分着色分析(基于不包含水分子的“干”蛋白结构),结果如图3左图所示。可以观察到,在其异喹啉酮片段的5位(图中红色圆圈高亮处),分子表面呈现红色,表明该区域的静电势与蛋白质口袋不互补。相比之下,在相同位置引入氟原子后得到的化合物6b,其对应区域的EC打分着色转变为绿色(图3右),这意味着氟原子的引入显著改善了该位点的静电互补性。由此可见,通过计算和可视化EC打分,研究人员能够快速、直观地将异喹啉酮片段的5位识别为一个通过引入氟原子有望显著提升活性的潜在优化位点,从而为理性的氟扫描设计提供了有力的计算依据。
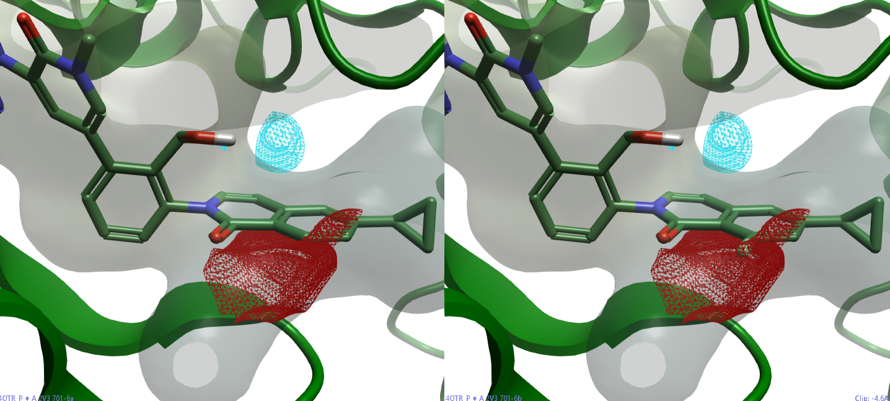
图4. BTK(PDB 4OTR)的蛋白场。飘带:BTK;红色:PIP +ve = 7.0;青蓝色:PIP -ve = 7.0;棍棒模型(左):6a;棍棒模型(右):6b。
通过对蛋白与配体分别进行静电分析,可以进一步从静电分布的根源上解释EC打分差异的成因。图4展示了化合物6b与BTK的共晶结构(PDB 4OTR)中,在6b的5-氟异喹啉酮片段周围5Å范围内的蛋白静电场分布(基于不包含结晶水的“干”蛋白计算)。可以观察到,在6a的异喹啉酮环5位碳原子C-H所指的方向上(图4左),存在一个红色的正静电势区域;而6b的氟原子(图4右)恰好位于这个正静电势环境之中,这为氟原子(带有部分负电)与蛋白质之间产生有利的静电吸引提供了基础。
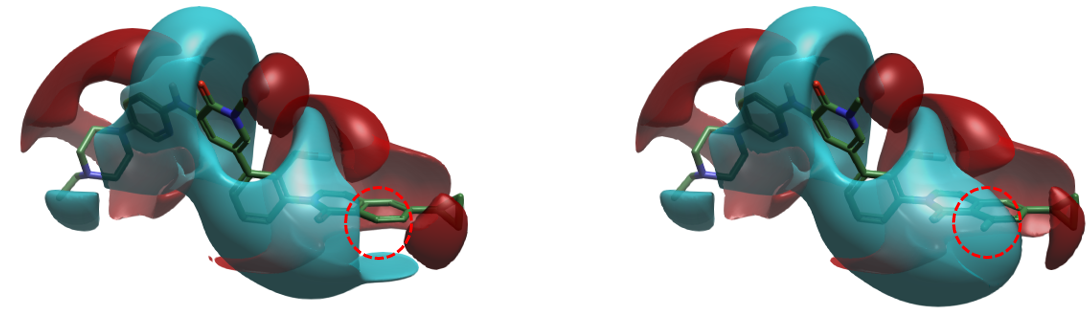
图5. BTK抑制剂6a(左)与6b(右)的配体场。配体场,红色:+ve = 2.0;青蓝色:-ve = 2.0
图5则展示了6a与6b的配体场。对比可见,在C-F键的方向上,6a的相应位置未呈现明显的负静电势区域(图5左),而6b的氟原子则引入了一个显著的青蓝色负静电势区域(图5右)。这一分析直观地表明:6b的氟原子所携带的局部负静电势,恰好与蛋白质结合口袋中特定的正静电势区域在空间上互补;而6a在同一位置因缺乏此负静电势,导致静电冲突。这从根本上解释了为何6b在该位点的EC打分表现为互补(绿色),而6a为冲突(红色)。
在基于静电互补性(EC)的分析中,我们通常使用不包含水分子的“干”蛋白结构进行计算。然而,在实际的生理环境中,结合口袋内水分子网络对相互作用的形成至关重要。如图2所示,化合物6b的氟原子与结合水分子HOH807的氧原子距离为3.4Å,这表明水分子介导的相互作用在实际结合中扮演了重要角色。由于水分子的动态性和取向不确定性,其静电贡献难以直接计算,但可以通过水合自由能分析进行定量评估。
特定水分子的稳定化作用可以通过比较其在复合物状态(holo)与无配体状态(apo)下的溶剂化自由能差值(ΔΔGsolv,公式1)来量化。若ΔΔGsolv小于0,则表明复合物的形成稳定化了该水分子,或者说该水分子对结合有净的正贡献;反之,若大于0,则表示该水分子在结合过程中发生了去稳定化,或者说该水对复合物起到去稳定化的作用。
$$
\Delta \Delta G_{solv} = \Delta G_{solv}^{holo} – \Delta G_{solv}^{apo} \cdots(1)
$$
使用Flare的水分析模块5对6b与BTK的复合物(PDB 4OTR)进行3D-RISM6计算,得到HOH807的ΔΔGsolv= -3.47 kcal/mol,证实该水分子对6b的结合具有显著的稳定化作用。类似地,该水分子对6a的结合也有利,其ΔΔGsolv= -2.83 kcal/mol。
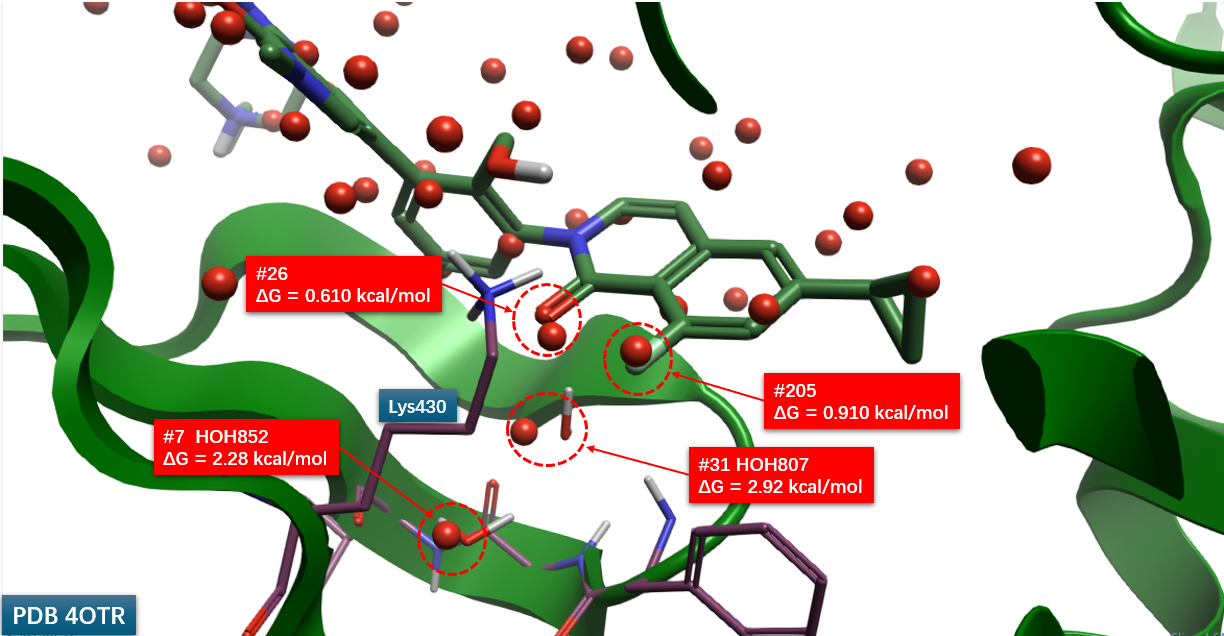
图6. 化合物6b与BTK共晶结构PDB 4OTR的apo-GIST水合位点。飘带:BTK;棍棒:6b;红色球形:apo-GIST水合位点(仅显示配体5Å范围之内)
水的分布信息同样可为理性氟扫描提供关键线索。通过对6b-BTK复合物(PDB 4OTR)进行无配体的GIST7分析(apo-GIST),可以预测apo状态下口袋内的水合位点及其热力学性质(图6)。分析发现,6b的氟原子恰好与一个预测的高密度水合位点(#205,ΔG = 0.91 kcal/mol)在空间上重合,同时也与蛋白的一个正范德华势区域重叠(未显示)。这证实,基于apo-GIST预测的、可被置换的能量不利水合位点,可以作为潜在的氟原子取代“热点”,因为用氟原子替代这类能量不利的水分子通常能获得结合自由能增益。
总结而言,在BTK抑制剂6b的案例中,静电互补性(EC)分析可快速定位潜在的氟取代优化位点,并通过蛋白/配体静电场进行归因解释;而水合作用分析(如GIST)则能从水分子稳定性和置换自由能的角度,为识别氟原子取代的有利位点提供独立且互补的热力学依据。 这两种计算方法的结合,为基于结构的理性氟扫描提供了更全面、更可靠的设计策略。
文献
- Lou, Y.; Sweeney, Z. K.; Kuglstatter, A.; Davis, D.; Goldstein, D. M.; Han, X.; Hong, J.; Kocer, B.; Kondru, R. K.; Litman, R.; McIntosh, J.; Sarma, K.; Suh, J.; Taygerly, J.; Owens, T. D. Finding the Perfect Spot for Fluorine: Improving Potency up to 40-Fold during a Rational Fluorine Scan of a Bruton’s Tyrosine Kinase (BTK) Inhibitor Scaffold. Bioorg Med Chem Lett 2015, 25 (2), 367–371. https://doi.org/10.1016/j.bmcl.2014.11.030.
- Lou, Y.; Han, X.; Kuglstatter, A.; Kondru, R. K.; Sweeney, Z. K.; Soth, M.; McIntosh, J.; Litman, R.; Suh, J.; Kocer, B.; Davis, D.; Park, J.; Frauchiger, S.; Dewdney, N.; Zecic, H.; Taygerly, J. P.; Sarma, K.; Hong, J.; Hill, R. J.; Gabriel, T.; Goldstein, D. M.; Owens, T. D. Structure-Based Drug Design of RN486, a Potent and Selective Bruton’s Tyrosine Kinase (BTK) Inhibitor, for the Treatment of Rheumatoid Arthritis. J Med Chem 2015, 58 (1). https://doi.org/10.1021/jm500305p.
- Flare (Version 11). https://cresset-group.com/software/flare
- Bauer, M. R.; Mackey, M. D. Electrostatic Complementarity as a Fast and Effective Tool to Optimize Binding and Selectivity of Protein–Ligand Complexes. J Med Chem 2019, 62 (6), 3036–3050. https://doi.org/10.1021/acs.jmedchem.8b01925.
- Flare Water analysis. https://cresset-group.com/software/flare-3drism
- Luchko, T.; Gusarov, S.; Roe, D. R.; Simmerling, C.; Case, D. A.; Tuszynski, J.; Kovalenko, A. Three-Dimensional Molecular Theory of Solvation Coupled with Molecular Dynamics in Amber. J Chem Theory Comput 2010, 6 (3), 607–624. https://doi.org/10.1021/ct900460m.
- Nguyen, C. N.; Kurtzman Young, T.; Gilson, M. K. Grid Inhomogeneous Solvation Theory: Hydration Structure and Thermodynamics of the Miniature Receptor Cucurbit[7]Uril. Journal of Chemical Physics 2012, 137 (4), 973–980. https://doi.org/10.1063/1.4733951.



