摘要:本文以Schrodinger公司MALT1别构抑制剂SGR-1505的发现为例,对比高成本FEP+计算与Flare平台静电互补性(EC)分析的效率与指导价值。结果表明,EC评分不仅快速、直观,还能准确预测活性趋势,为结构优化提供精准指导。
Schrodinger 公司 Nie 等人(2025)近期发表的研究详细阐述了其 MALT1 别构抑制剂 SGR-1505(化合物 26,见图 1)的发现过程。
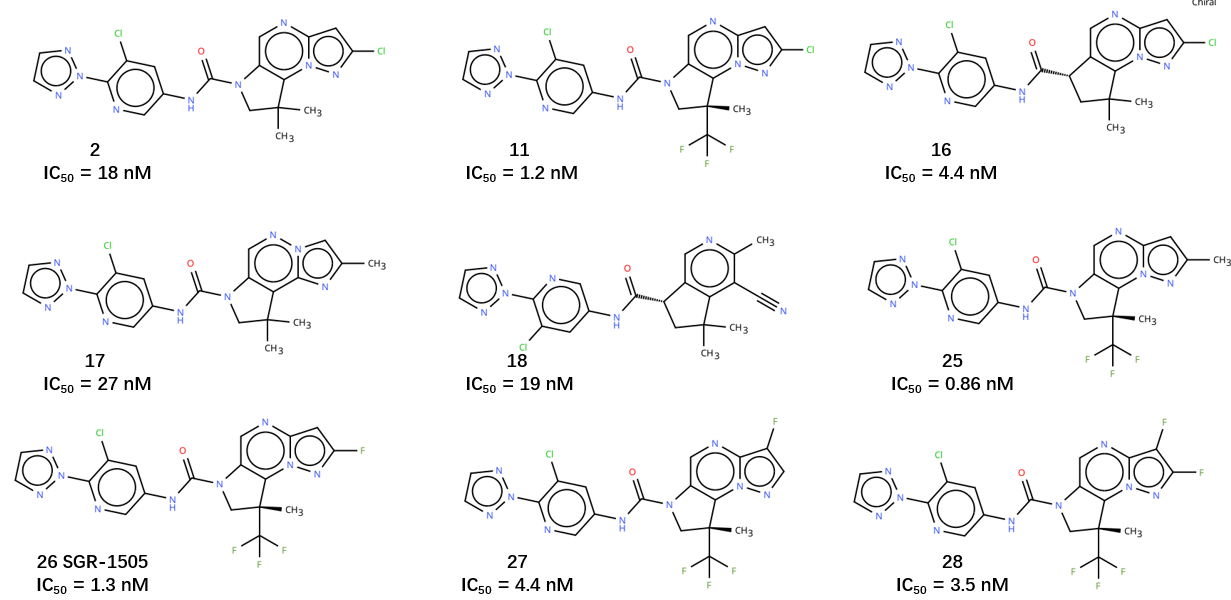
图 1. 一系列形状相似的 MALT1 抑制剂类似物
总体而言,该研究体现了典型的跨学科协作模式:计算化学团队负责 FEP+(自由能微扰)建模与虚拟化合物库的枚举,药物化学团队则基于计算预测结果设计合成路线;双方通过实时数据共享实现快速迭代。例如,化合物 11 的合成曾面临显著挑战(尝试了 11 条不同路线),最终在计算模型提供的高置信度预测支持下得以成功克服。
研究中集成多种计算技术,实现了从广义化学空间探索到多参数优化(MPO)评分的无缝衔接,显著提升了先导化合物优化的决策效率。具体而言,在项目周期内共对约 80 亿个分子设计进行了计算评估;其中约 6000 个化合物通过 FEP+ 进行了 MALT1 抑制活性的定量预测;最终,129 个化合物(包括 78 个属于先导系列的分子)被优先用于合成与实验验证。
In summary, over the course of the project, ∼8 billion ideas were evaluated in silico; among these, ∼6000 ideas were evaluated by FEP+ for MALT1 potency prediction. A total of 129 compounds (78 compounds in the lead series) were prioritized for synthesis during the course of the project.
然而,FEP+ 计算的成本亦相当高昂:每个模拟需运行 25 纳秒,并采用 24 个 λ 窗口。在开展前瞻性设计之前,研究团队还进行了回顾性验证,以确保所用协议能够准确复现实验数据:
FEP+ simulations were performed for 25 ns using 24 lambda windows. Retrospective studies were performed to ensure that the protocol was able to recapitulate experimental data prior to profiling of new design ideas.
由此可见,FEP+ 是一个计算周期长、资源消耗大的方法,其高昂成本使得多数研究团队难以广泛采用。为此,本文将介绍一种更为高效且经济的替代方案:Flare 药物设计平台中的蛋白–配体静电互补性(Electrostatic Complementarity, EC)分析。
静电互补性打分(EC score)用于量化配体与蛋白结合口袋之间的静电势匹配程度。其核心原理简洁而直观:当配体与受体的静电势在空间上呈现等量异号(即配体带负电区域对应蛋白带正电区域,反之亦然)时,二者可实现最大化的静电亲和力。
Bauer 等人(2019)的研究已表明:当系列类似物间的活性差异主要源于静电性质变化时,EC 评分与实验测得的结合亲和力高度相关。
以 Nie 等人(2025)研究中的化合物 2 与 11 为例:二者结构仅在某一取代基上存在差异——化合物 2 含甲基,而化合物 11 对应位置为三氟甲基。这一微小修饰却使 MALT1 抑制活性提升近 10 倍(IC₅₀ 从 18 nM 降至 1.2 nM)。利用 Flare 对化合物 11 与 MALT1 的共晶结构(PDB: 9MKE)进行分析,计算蛋白相互作用势(Protein Interaction Potential, PIP),结果如图 2 所示:甲基/三氟甲基所在区域恰好位于蛋白 PIP 的正静电势区。由于三氟甲基其表面呈现负静电势,与蛋白口袋的正电区域形成更优的静电互补,从而解释了化合物 11 的高活性。
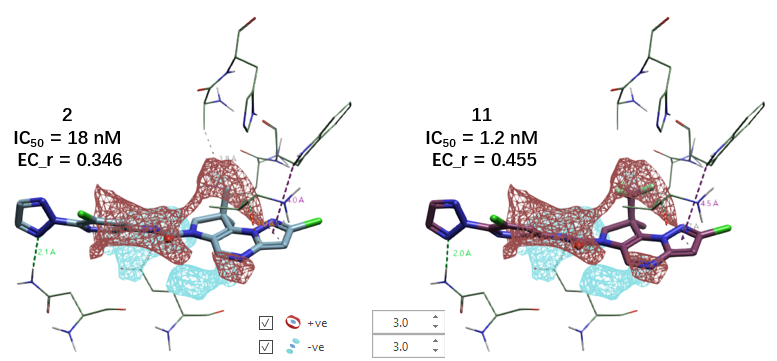
图 2. 化合物 2 与 11 与 MALT1 的结合模式。红色等值面:PIP 正静电势区;蓝色等值面:PIP 负静电势区
将 EC 打分映射至配体分子表面,可为结构优化提供直观、可视化的指导:绿色区域表示静电互补良好,红色区域则提示存在静电冲突。该方法的操作逻辑简洁:识别配体表面的红色(冲突)区域,并通过结构修饰(如引入吸电子或供电子基团)将其转化为绿色(互补)区域。相较于 FEP+,EC 分析不仅计算速度更快、成本更低,且能明确指出分子中需优化的具体位置——而 FEP+ 仅提供整体结合自由能,无法定位局部问题。
以化合物 2 与 11 为例(图 3):化合物 2 的甲基区域显示为深红色(EC 打分 EC_r = 0.346),而化合物 11 的三氟甲基区域则呈现绿色(EC_r = 0.455)。这一趋势与其实验 IC₅₀ 值高度一致,表明 EC 表面不仅能识别需优化的结构片段,还可合理预测活性变化趋势。
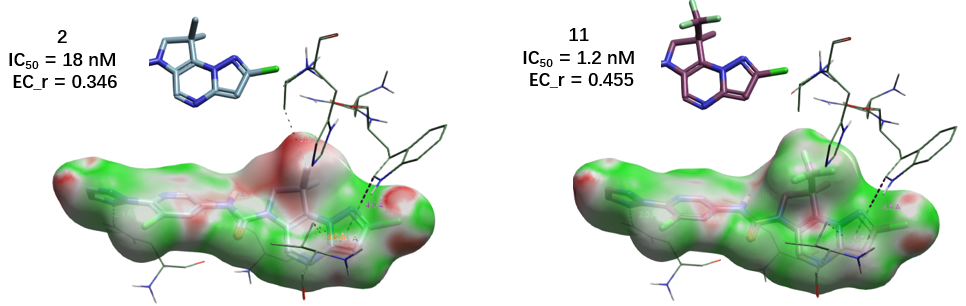
图 3. 化合物 2 与 11 的静电互补性分子表面着色图
进一步地,在图 1 所示的 9 个结构相似的 MALT1 抑制剂衍生物上,Flare 的 EC 分析同样展现出良好的预测能力。计算所得 EC 评分与分子表面着色结果如图 4 所示。
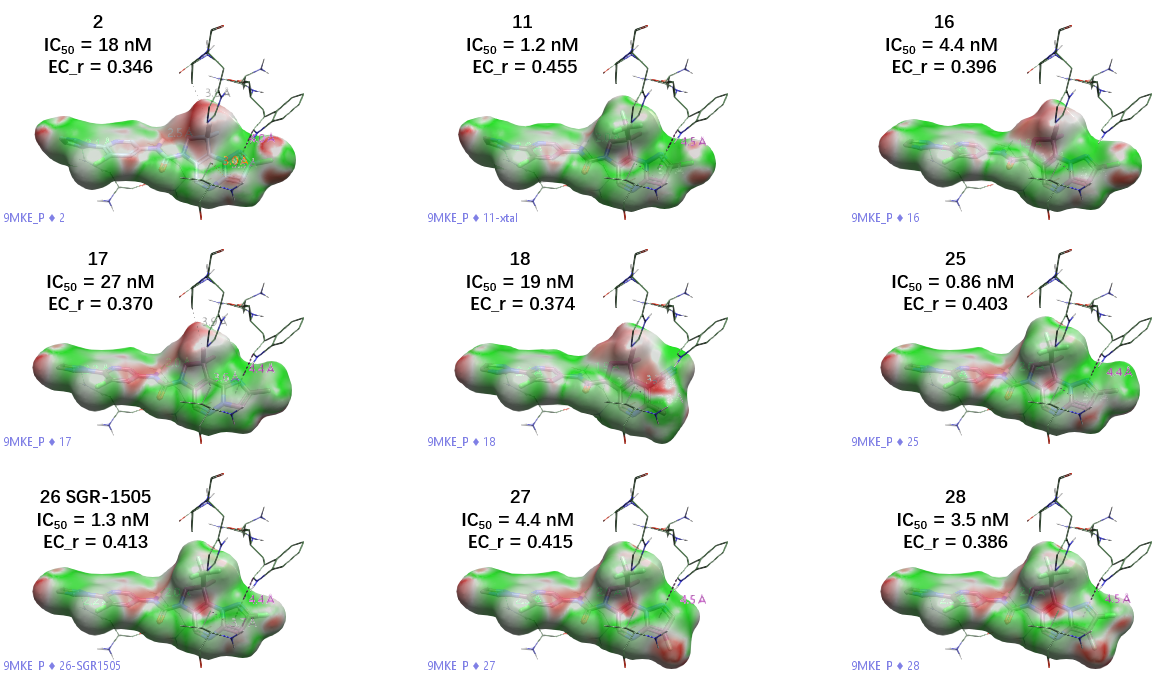
图 4. 9 个 MALT1 抑制剂的静电互补性分子表面。绿色:静电互补;红色:静电冲突。
值得注意的是,这 9 个化合物的 EC 打分与其 MALT1 pIC50值之间呈现出显著的线性相关性(Pearson 相关性系数 R² = 0.621,见图 5)。其中,活性最低的三个化合物(2、17、18)具有最低的 EC 评分,并在图中明显聚集成簇,与高活性化合物清晰分离。
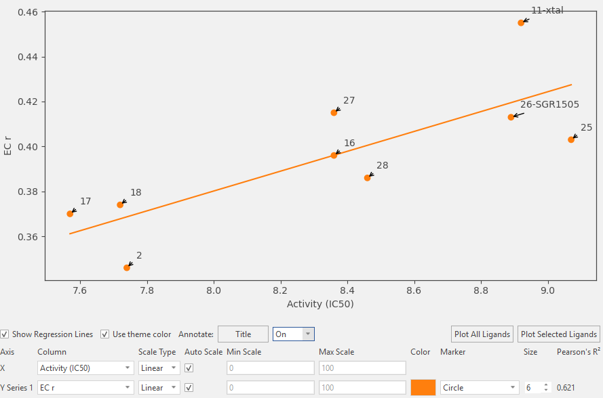
图 5. 9 个 MALT1 抑制剂的 EC 打分与 pIC50 值的相关性分析。
为进一步验证静电互补性差异的物理根源,可对配体分子表面按其静电势着色(图 6):化合物 2 的甲基区域呈现深红色(正静电势),与蛋白 PIP 的正电区域(图 2)发生静电排斥冲突;而化合物 11 的三氟甲基区域则呈现蓝色(负静电势),与蛋白口袋正电区域形成有利的静电互补。
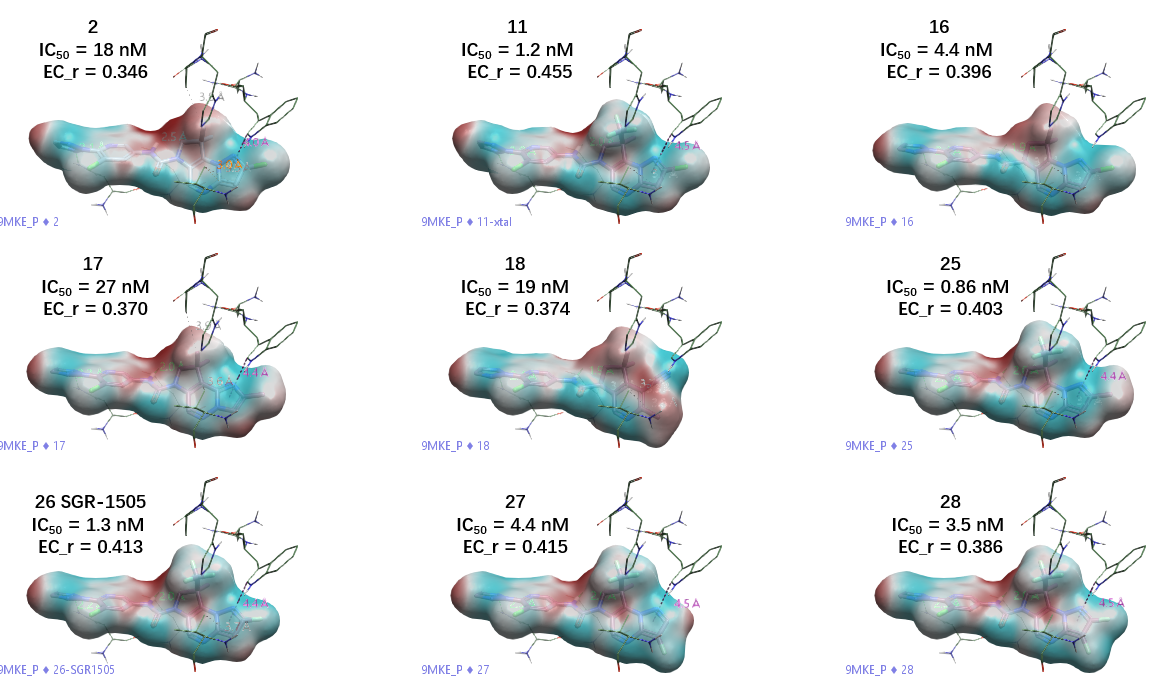
图 6. 9 个 MALT1 抑制剂的静电势表面着色图。红色:正静电势;蓝色:负静电势。
综上所述,Flare 平台的静电互补性(EC)分析是一种快速、高效且直观的计算工具,能够精准识别先导化合物中存在静电冲突的结构片段,为提升蛋白–配体结合亲和力提供明确的结构优化方向。在资源有限或需快速迭代的药物设计场景中,EC 分析可作为 FEP 等高成本方法的有效补充乃至替代策略。
推荐阅读
- Bauer等人的EC方法学文章:https://doi.org/10.1021/acs.jmedchem.8b01925
- 用静电互补性快速、高效地优化配体-蛋白复合物的结合与选择性
- 如何用静电互补性打分
在自己的项目中使用静电互补性分析
静电互补性分析是药物设计平台Flare的一个模块,最新版Flare V11 引入了强大的新科学能力、更快的工作流和增强的易用性,为您提供高效、精准探索复杂体系的工具。
立即联系我们申请试用,体验 Flare 的最新功能。我们的专家团队将指导您完成安装与设置,同时我们丰富的教程库(从基础工作流到高级方法)确保您顺利上手。借助 Flare V11,您将能够更快推进研究、深入洞察机制,并设计出最具价值的分子。
联系我们: 020-38261356 info@molcalox.com
参考文献
- Nie, Z. et al. (2025) “Accelerated In Silico Discovery of SGR-1505 : A Potent MALT1 Allosteric Inhibitor for the Treatment of Mature B-Cell Malignancies,” Journal of Medicinal Chemistry, 68(22), pp. 23977–23992. Available at: https://doi.org/10.1021/acs.jmedchem.5c01494.
- Bauer, M.R. and Mackey, M.D. (2019) “Electrostatic Complementarity as a Fast and Effective Tool to Optimize Binding and Selectivity of Protein–Ligand Complexes,” Journal of Medicinal Chemistry, 62(6), pp. 3036–3050. Available at: https://doi.org/10.1021/acs.jmedchem.8b01925.



