前言
自由能微扰(FEP)被认为是估算小分子结合亲和力的金标准模拟方法,该指标对药物发现至关重要。FEP的准确性高度依赖于蛋白质-配体复合物的精确模型,这是其基础分子动力学模拟的初始条件。这一要求限制了FEP在药物发现早期阶段的应用——该阶段往往缺乏合适的实验晶体结构。以Boltz-2为代表的新一代结构预测模型,有望通过预测蛋白质-配体复合物结构来突破此局限。
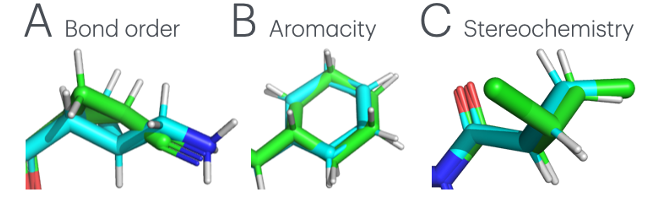
图1. Boltz-1生成的配体结构中常见的化学不准确性及优化策略的效果。Boltz-1有时会错误地建模输入的SMILES字符串,导致(A)错误的键级、(B)不适当的芳香性或(C)不正确的立体化学构型。
然而,以Boltz为代表的结构预测模型存在一个致命的问题:预测的蛋白质-配体复合物结构中的配体化学错误,图1。这些错误包括:
- 不正确的键级
- 不适当的芳香性
- 错误的立体化学构型
在Recursion与Valence Labs联合发表预印版文章《Boltz-ABFE: Free Energy Perturbation without Crystal Structures》中提出用POSIT重对接(redocking)来解决这个问题1。
配体构象校正工具
POSIT是OpenEye开发的一种基于模板的分子对接方法2,3,在Boltz-ABFE流程中被用于重新对接(re-docking)步骤,以纠正Boltz预测的蛋白质-配体复合物结构中的配体化学错误。这些错误包括:(1)不正确的键级 ;(2)不适当的芳香性;(3)错误的立体化学构型。
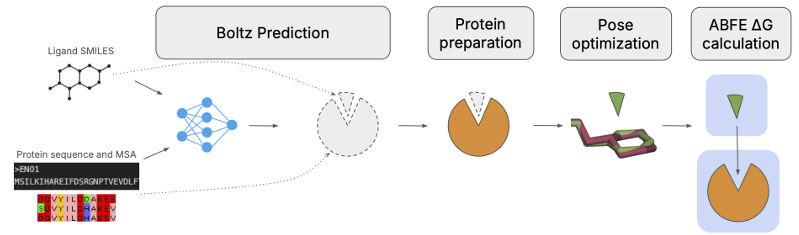
图2. Boltz-ABFE工作流
工作原理
POSIT的工作机制包括:
- 首先使用最大公共子结构(MCS)覆盖对目标(初始)和模板(Boltz)构象进行叠合
- 然后进行基于形状和药效团的拟合和优化
- 能够忠实地重现模板的位置和几何形状
在Boltz-ABFE工作流中的优势
研究发现,与另一种Hybrid对接方法相比,POSIT在计算和实验结合自由能之间取得了更好的一致性,POSIT生成的构象在后续的绝对结合自由能(ABFE)计算中表现更优,因此POSIT被选为Boltz-ABFE流程中配体化学纠正的首选方法。
局限性
POSIT方法也存在一定限制,当Boltz预测包含错误的立体化学时,POSIT对刚性形状保持的张力能可能会产生不利的构象。这种情况下,生成的构象可能不适合后续的分子动力学模拟。
研究应用
在Boltz-ABFE研究中,POSIT被应用于:
- Boltz-1预测结构的重新对接(“Boltz-1+P”)
- Boltz-2预测结构的重新对接(“Boltz-2+P”)
- 与晶体结构作为起点的ABFE模拟结果进行比较
总之,POSIT方法在Boltz-ABFE研究中作为关键的配体构象校正工具,帮助研究人员在没有实验晶体结构的情况下,通过校正预测结构中的配体化学错误,为后续的分子动力学模拟和自由能计算提供更准确的初始结构,从而扩展了自由能扰动(FEP)方法在药物发现早期阶段的应用范围。
文献
- Thaler, S. et al. (2025) “Boltz-ABFE: Free Energy Perturbation without Crystal Structures.” Available at: http://arxiv.org/abs/2508.19385.
- https://www.eyesopen.com/posit
- Kelley, B.P. et al. (2015) “POSIT: Flexible Shape-Guided Docking for Pose Prediction,” Journal of Chemical Information and Modeling, 55(8), pp. 1771–1780. Available at: https://doi.org/10.1021/acs.jcim.5b00142.



