摘要:设置盐浓度以使得结合测定的实验条件与分子动力学(MD)或自由能微扰(FEP)模型相匹配,可以显著提高模拟的准确性,特别是对于带电配体,可以改进结合亲和力的预测。本文以FEP准测试基集的TYK2数据集带有四氮唑基团的配体33为例,使用三种不同的方式运行10ns的MD:在溶液中,在设定为“仅中和”的复合物中,以及在离子强度为150mM的复合物中。结果表明,当使用“仅中和”时四氮唑环在结合位点不太稳定;当离子强度设定为150mM时,带电的四氮唑环显著地更稳定。总的来说,在本研究中,我们证明了模拟测定条件离子强度的重要性,特别是当配体带电荷时。
作者:Lauren Nelson/2024-05-22
编译:肖高铿
设置盐浓度以使得结合测定的实验条件与分子动力学(Molecular Dynamics,MD)或自由能微扰(Free Energy Perturbation,FEP)模型相匹配,可以显著提高模拟的准确性1。特别是对于带电配体,可以改进结合亲和力的预测。Cresset最近的工作集中在FEP计算中配体电荷变化的转换,这已在Flare V8中实现,特别是考虑到TYK2数据集2。该数据集包含两个带负电荷的配体:一个带有羧基(配体“32”),另一个带有四氮唑基团(配体“33”),见图1,与其它电中性的配体一起构成数据集。本文将重点关注配体33的分子动力学(MD)研究。
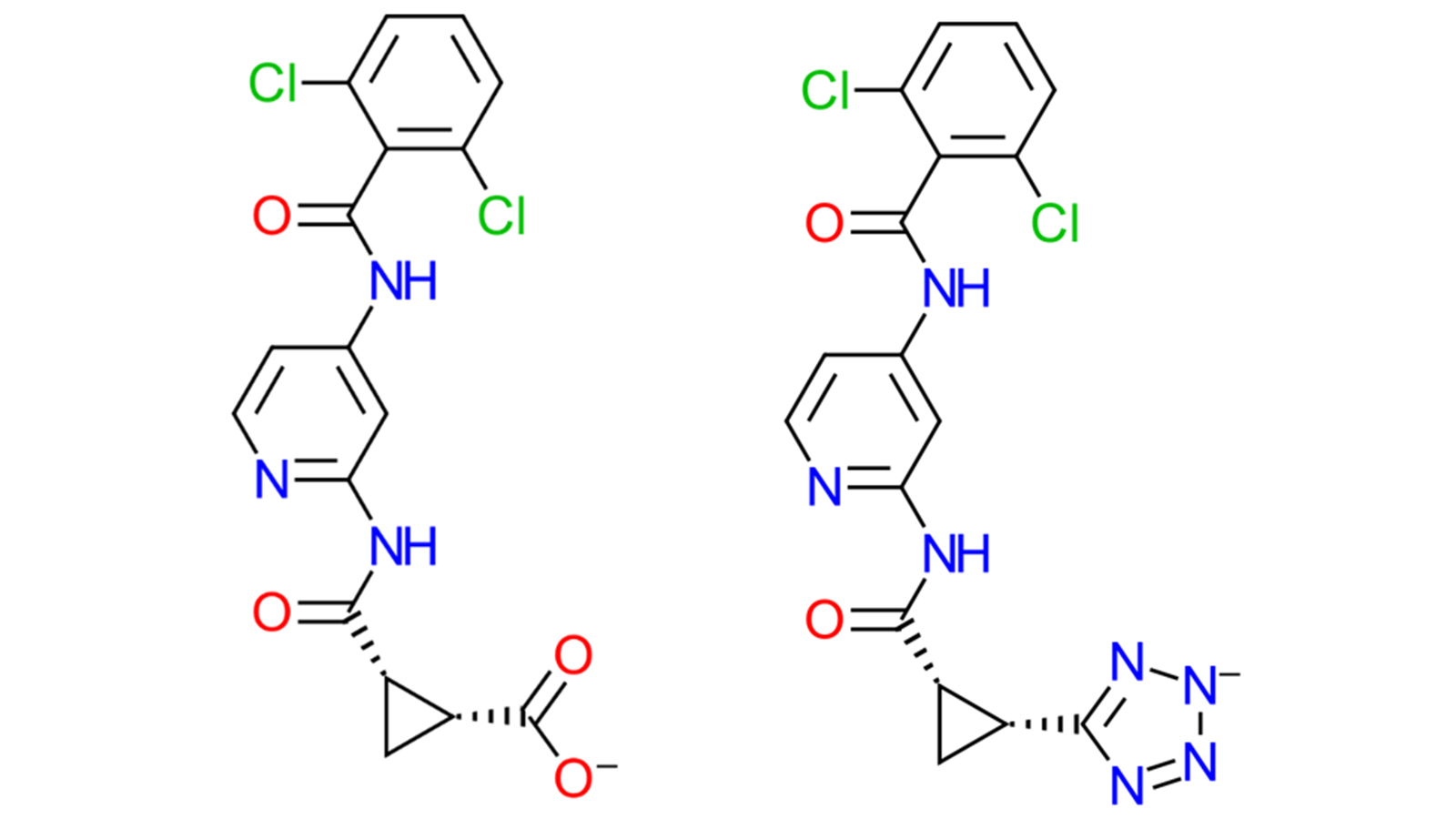
图1. TYK2数据集2中的两个带电配体:带有羧基的配体32(左)和带有四氮唑的配体33(右)
带电配体的分子动力学模拟
在本文中,我们研究了与简单的中和体系(不添加盐浓度)相比,将离子强度(即NaCl盐浓度)设定为150mM对配体33的动力学影响。在“Dynamics calculation”控制面板的“More options”中,有用于高级设置的选项,如图2所示。一种选择是“仅中和(Just neutralize)”体系的默认选项,而另一种选择允许手动调整。在这种情况下,将之设置为150mM以更好地模拟测定条件3。该体系的动力学实验使用三种不同的方式运行10ns:在溶液中,在设定为“仅中和”的复合物中,以及在离子强度为150mM的复合物中。
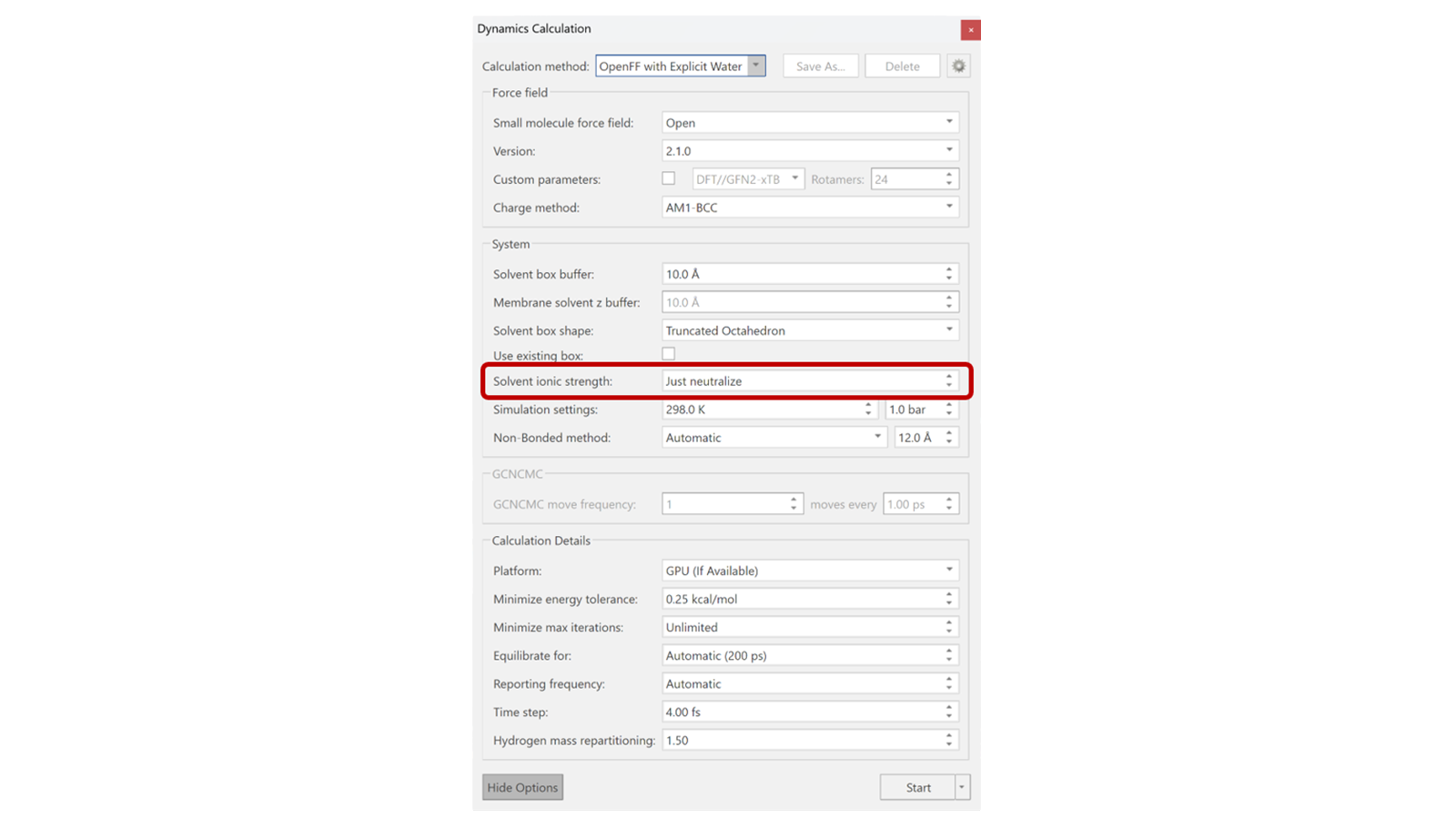
图2. Flare的分子动力学选项,特别突出了溶剂离子强度
Flare的MD分析
当动力学运行完成时,会显示一条MD轨迹,提供了一种简单的方法来可视化模拟中各种成分的RMSD。检查配体RMSD是一种可靠的方法,可以确保所讨论的配体在复合物中是稳定的,并且按预期执行,特别是在准备FEP计算时。例如,RMSD值的大幅或突然变化,表明与初始配体帧的高度偏离,可能意味着配体发生了巨大移动,甚至可能与结合位点分离。在这种情况下,如图3所示,将配体33的“仅中和”体系与离子强度设置为150mM体系的RMSD进行比较,我们可以识别出四氮唑环在模拟中发生翻转的帧。
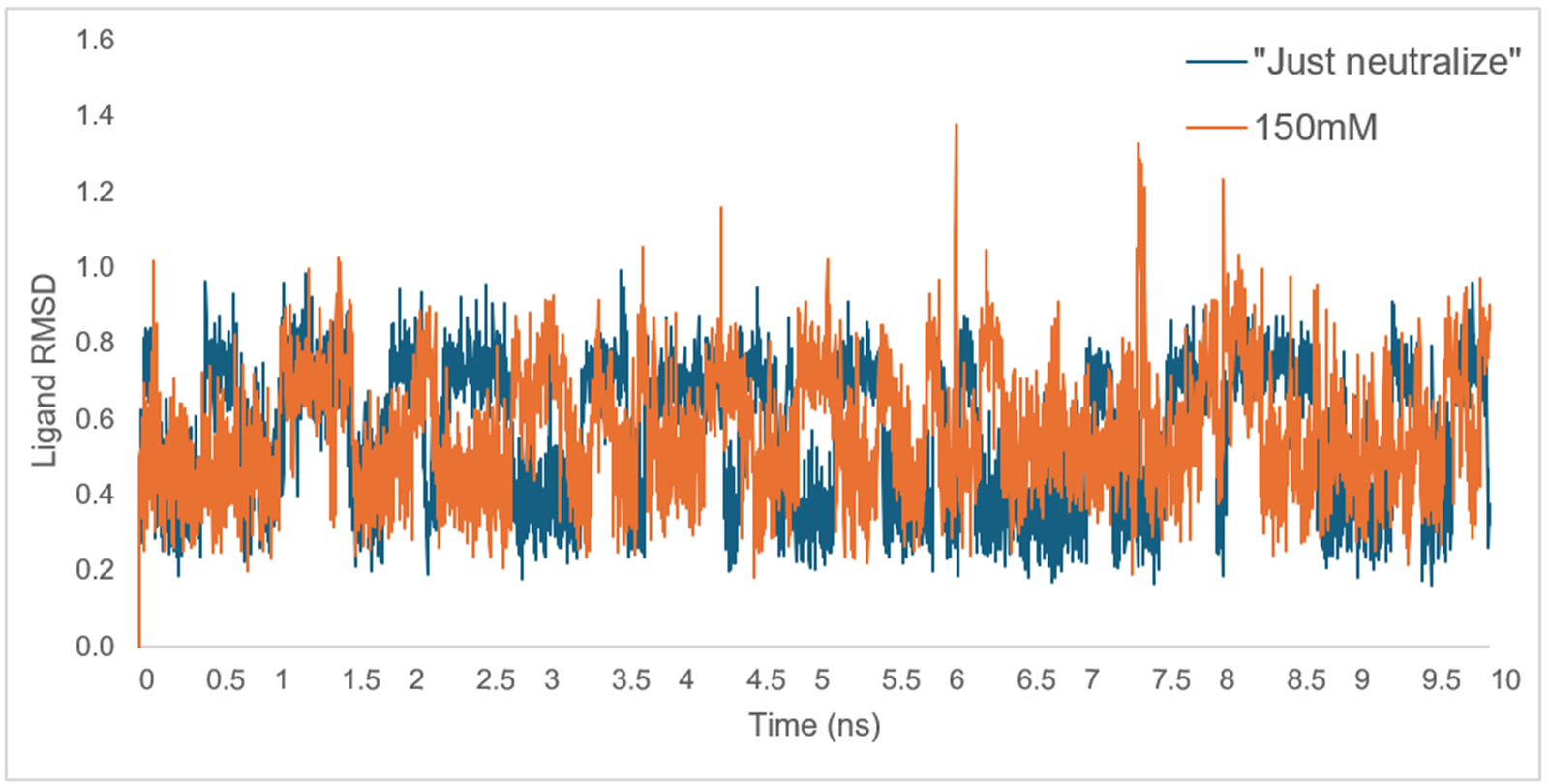
图3. 配体重原子RMSD的示意图,描述了配体33的两个10ns动力学计算:离子强度设置为“仅中和”(蓝色)和150mM(橙色)
除了RMSD之外,Flare的动力学分析还提供了配体与附近残基(包括水分子)之间发生接触次数的分解。专注于蛋白质-配体复合物的两个MD模拟,识别出配体33和ARG13之间的关键结合相互作用。通过比较四氮唑环和ARG13之间的接触,结果表明,与使用“Just neutralize”时产生的相互作用相比,尽管当施加150mM的离子强度时发生的相互作用数量较少,但这些相互作用更加稳定,因为它们在MD帧中占有更高的百分比。这种行为可见表1的A和B部分所示。
表1. 在10ns动力学模拟期间配体33的四唑氮与ARG13蛋白残基之间出现氢键和盐桥相互作用的帧数百分比,其中(A)为“仅中和”体系,(B)为150mM离子强度体系。
(A) “Just neutralize”体系
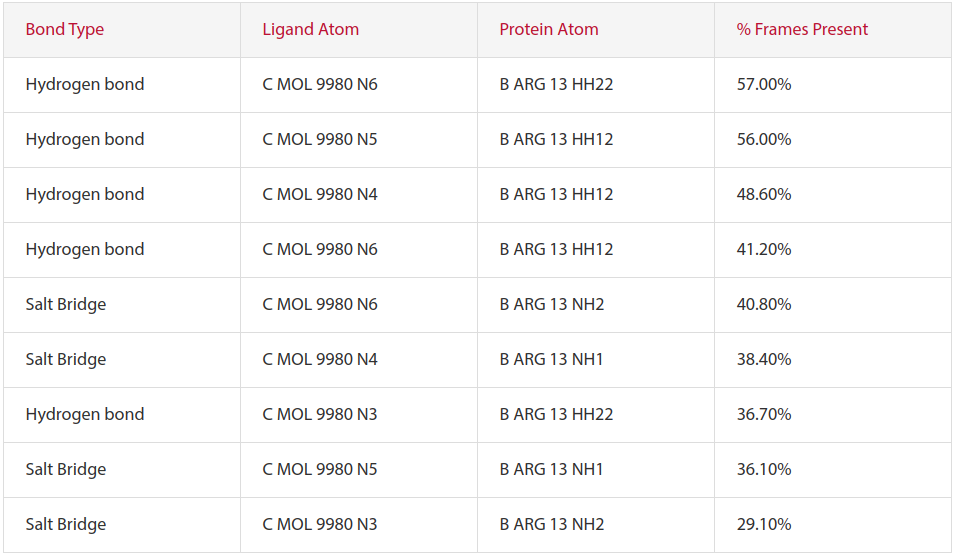
(B) 150mM离子强度体系
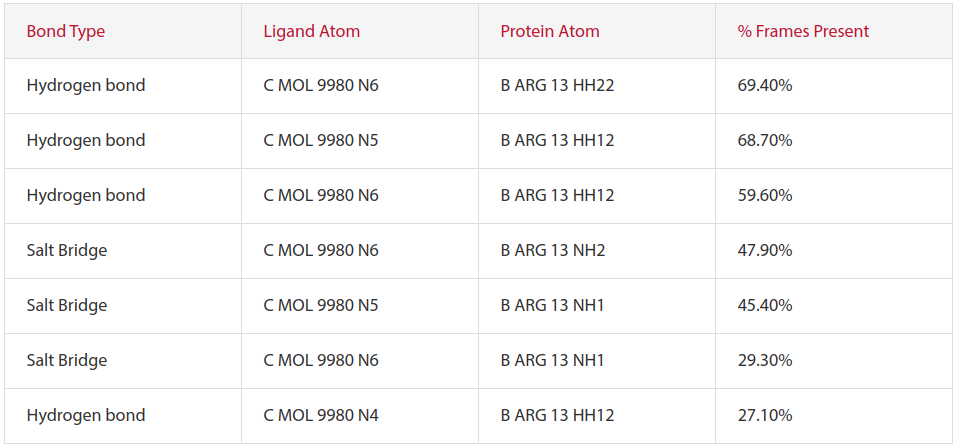
为了进一步探索配体RMSD的差异和接触次数的减少,我们在3D视图中分析了轨迹输出。我们可以使用配体RMSD图来识别四氮唑环可能发生翻转的帧。从表1中可以看出,四氮唑N5、N6与ARG13之间的相互作用最为突出,因此在复合物MD模拟开始时,如图4所示,测量了两个体系这两个点之间的距离。
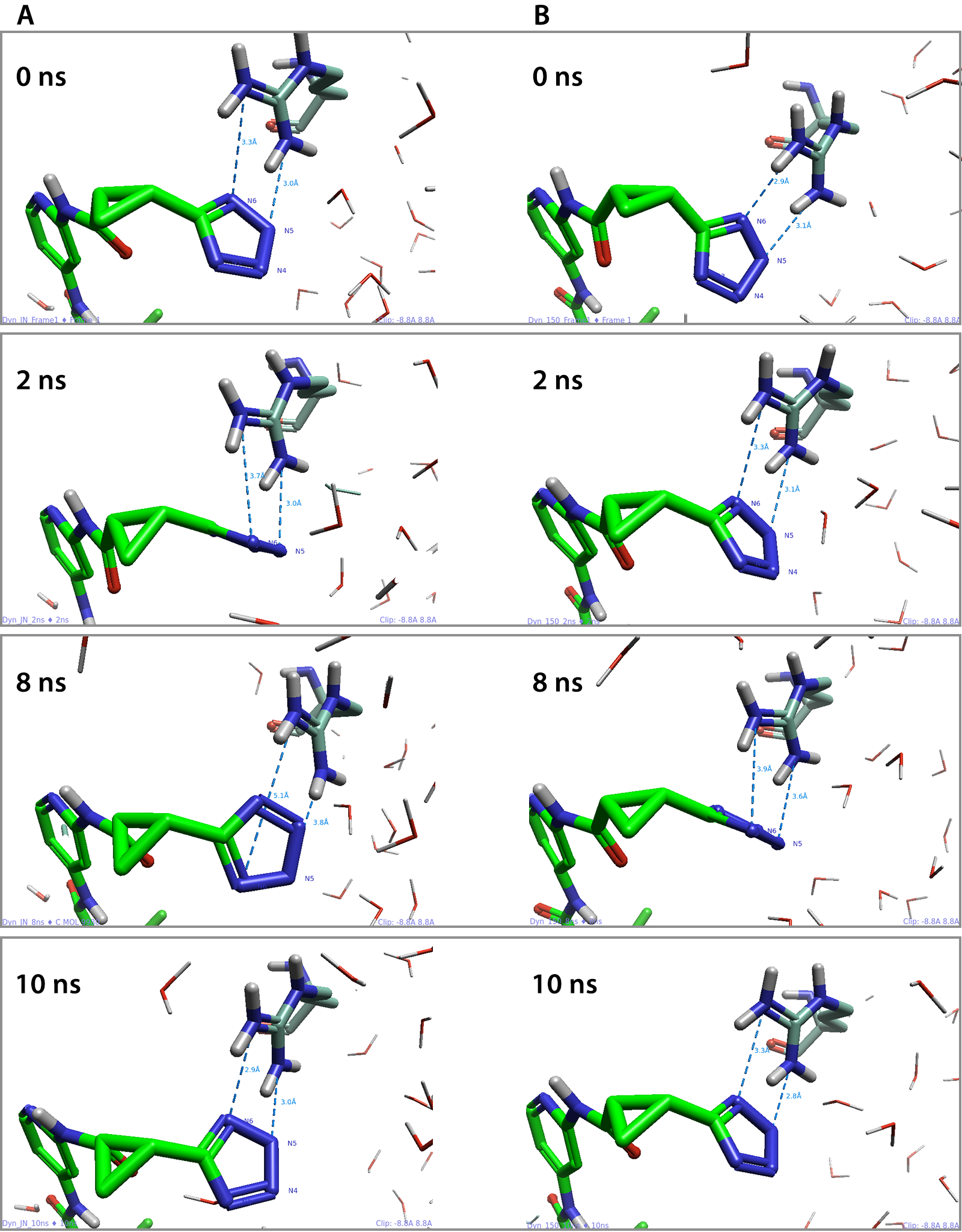
图4. 在(A)“Just neutralize”和(B)150mM离子强度模拟中,在0、2、8和10ns处测量了四氮唑N5、N6与ARG13残基之间距离
通过研究在两个模拟过程中蛋白质-配体的测量结果,我们能够证明与离子强度设定为150mM体系相比,在”仅中和”体系的MD模拟过程中,四氮唑环的稳定性较差。这是显而易见的,因为在3D视窗内观察到四氮唑环翻转的增加,,从而与环另一侧的N4和N3(表1,A)产生更多不同的接触。
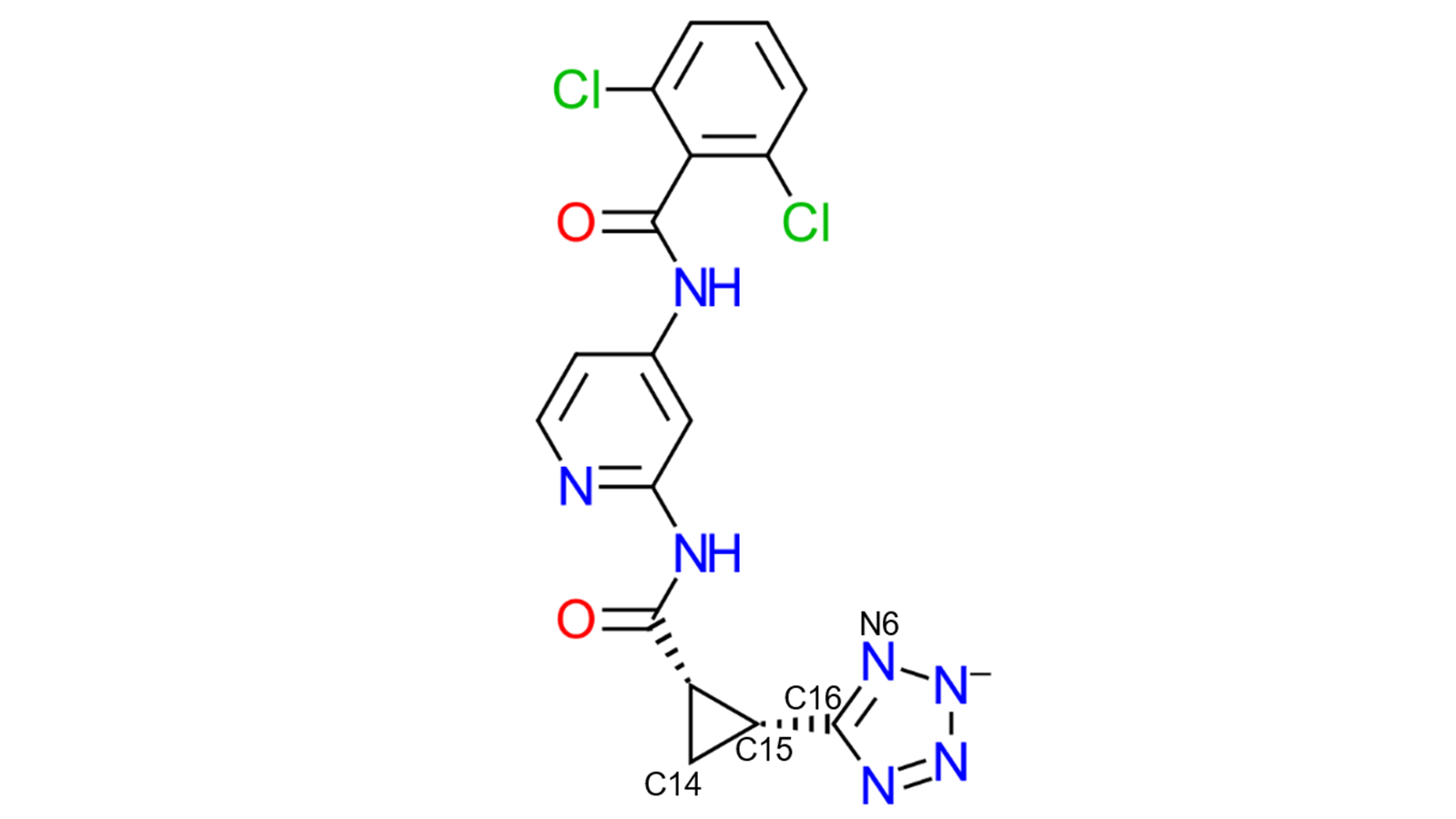
图5. 在三个MD模拟中测量扭转角(C14-C15-C16-N6)以进行比较。
最后,为了进一步证明当使用“仅中和”时四氮唑环在结合位点不太稳定,考察了图5中高亮显示的扭转角(C14-C15-C16-N6)。为了进行比较,对溶液中的配体进行了一个10ns的动力学模拟。绘图,如图6所示,再次明显的是,当离子强度设定为150mM时,带电的四氮唑环显著地更稳定,因为扭转角在144-180°之间的分布比任何其他角度显著地多。相比之下,当使用“仅中和”时,观察到的扭转角变化较大,与配体33在溶液中时没有什么不同。
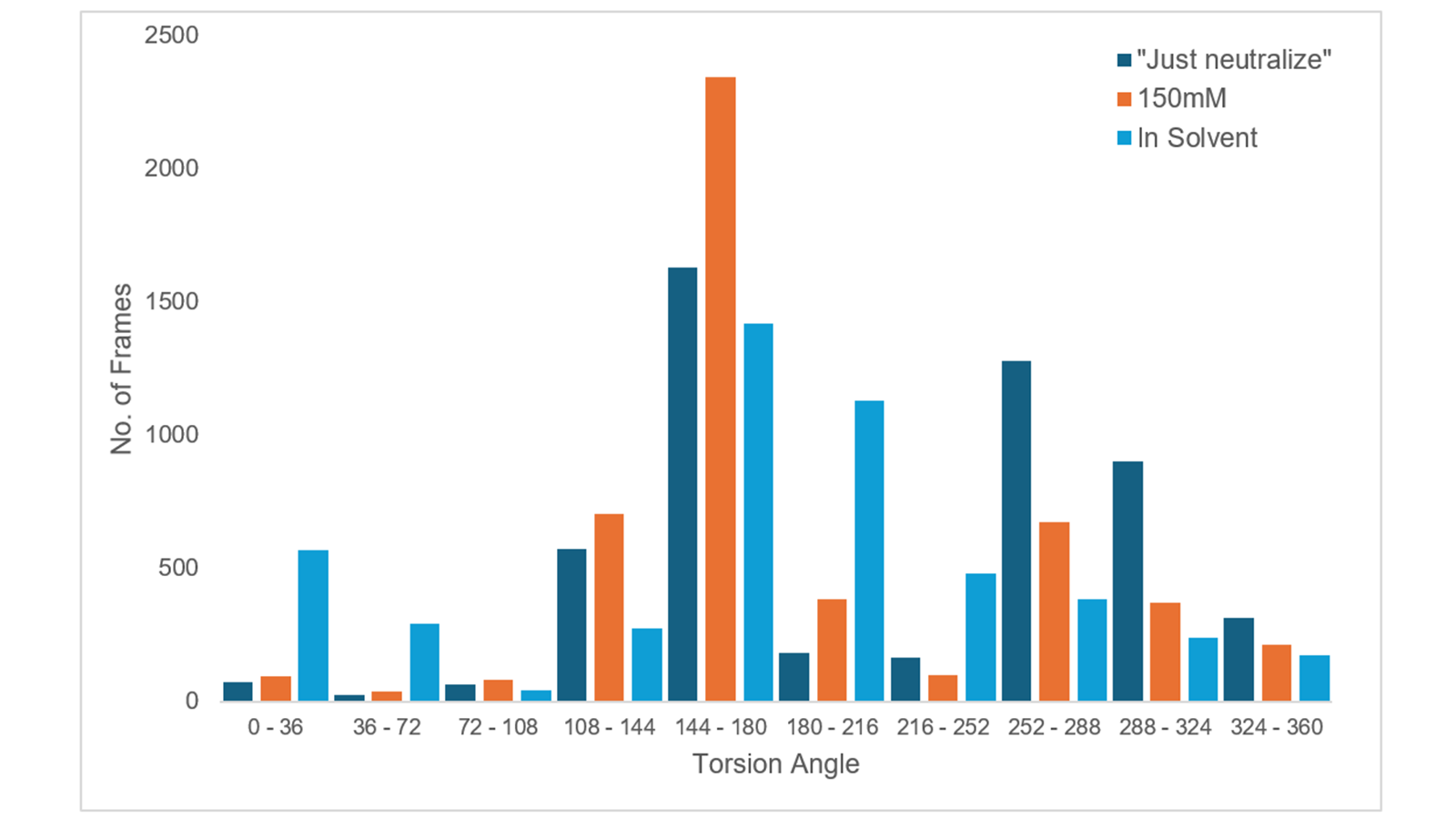
图6. 棒图描绘了配体33的四氮唑环在三个MD模拟中的扭转角(C14-C15-C16-N6)分布。深蓝色:“仅中和”,橙色:150mM离子强度,浅蓝色:溶液中的配体。
总的来说,在本研究中,我们证明了模拟测定条件离子强度的重要性,特别是当配体带电荷时,同时Flare提供了许多的分子动力学分析工具可供分析使用。
有关Flare分子动力学环境、工作流和分析工具的可视化演示,请索取观看我们的网络研讨会录像。
参考文献
- W. Chen et al. Accurate Calculation of Relative Binding Free Energies between Ligands with Different Net Charges. J. Chem. Theory Comput. 2018, 14, 6346-6358
- J. Liang et al. Lead Optimization of a 4‑Aminopyridine Benzamide Scaffold To Identify Potent, Selective, and Orally Bioavailable TYK2 Inhibitors. J. Med. Chem. 2013, 56, 4521−4536
- R. E. Farrell Jr. RNA and the Cellular Biochemistry Revisited. RNA Methodologies, 3rd edition. 2005, 1-16. Academic Press
联系我们、获取试用或商务合作
想要亲自计算或在自己的项目中使用Flare Dynamics,或者商务合作,请联系我们。



