摘要:对于初学者来说,诸如自旋多重度、闭壳层、限制性模型等量子化学术语的每一个都足以让人望而却步。本教程重点介绍了闭壳层体系、开壳层体系以及自旋多重度、自旋限制模型、自旋非限制模型等相关计算模型的基本概念。并以氧分子基态的计算为例,详细说明了如何利用Gaussian程序进行闭壳层和开壳层体系的计算。
作者:陈宇
日期:2017-12-15
关键字:闭壳层体系 开壳层体系 自旋限制模型 自旋非限制模型
一.基本概念
1. 闭壳层体系(closed shell systems)
是指在具有偶电子数的体系中,自旋向上(spin up)和自旋向下(spin down)的电子数相同,并且自旋相反的电子俩俩配对(图1)。对于闭壳层体系,自旋多重度总是M=1,也称为单重态(singlet)。对于任何体系自旋多重度的计算公式:
M=2S+1
其中M为自旋多重度,S为体系的总自旋量子数。
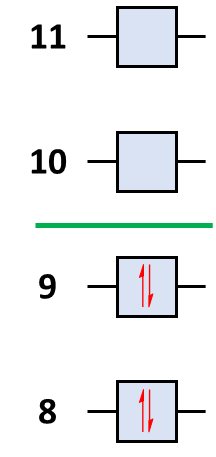
图1.闭壳层体系
2. 开壳层体系(open shell systems)
是指存在未配对电子的体系。通常分为两种情况,对于奇电子数体系,一定存在未配对电子,因此一定是开壳层体系(图2a);而对于某些偶电子数体系(例如氧分子),它的基态是三重态,此时体系中有两个未配对的电子(图2b),因此这种体系也称为开壳层体系。
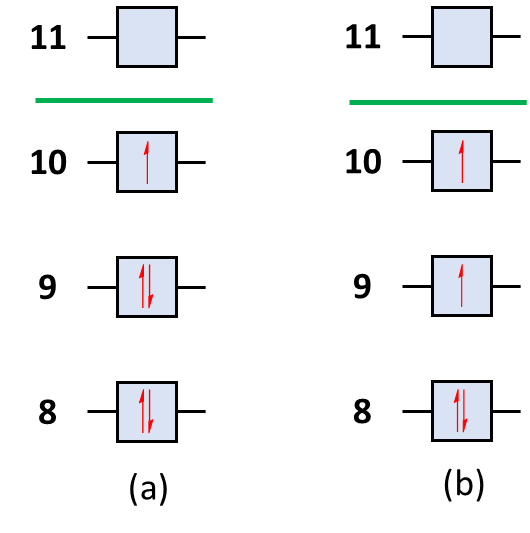
图2. 开壳层体系
3. 自旋限制模型(spin restricted model)
是指在实际计算分子轨道时,对于自旋向上与自旋向下的电子,使用同一组轨道。也就是说,在进行自洽场迭代(SCF)的过程中,只需要计算一种自旋的轨道,另一种自旋的电子直接填充在这个轨道中。
4. 自旋非限制模型(spin unrestricted model)
是指在实际计算分子轨道时,对于自旋向上和自旋向下的电子,各自采用不同的轨道。也就是说,自旋向上和自旋向下的电子都要分别进行自洽场迭代(SCF)的计算。因此在同等方法基组水平下,采用自旋非限制模型的计算量要大于自旋限制模型。
5. 自旋限制模型与自旋非限制模型的使用
- 对于闭壳层体系通常使用自旋限制模型。(需要注意的是,对于闭壳层体系,若使用自旋非限制模型,也能得到与使用自旋限制模型相同的结果,但计算量会增大,因此不建议使用)
- 对于开壳层体系需要使用自旋非限制模型。(对于开壳层体系若使用自旋限制模型,则不能得到正确的结果)
二.利用Gaussian程序模拟开壳层体系的具体步骤
Gaussian程序提供了调用自旋限制模型和自旋非限制模型的方法,用来模拟闭壳层和开壳层体系,下面我们将以氧气分子(O2)为例(具有偶电子数),详细说明如何使用这些方法,具体包括:
(1)假定基态氧分子的自旋多重度M=1,我们分别使用自旋限制模型和自旋非限制模型两种方法进行计算。
(2)假定基态氧分子的自旋多重度M=3(也就是三重态,Triplet),我们将使用自旋非限制模型进行计算。实际上,对于M≠1的体系,无法调用自旋限制模型进行计算。
1.计算自旋多重度M=1的氧分子体系
1.1 使用自旋限制模型
第一步:利用GaussView构建氧分子结构。
第二步:编辑输入文件。
利用自旋限制模型计算M=1的氧分子体系输入文件:
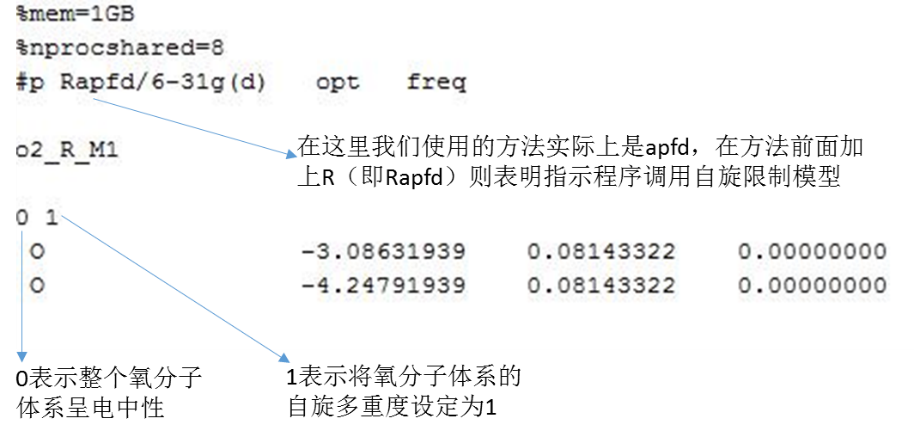
图3. 自旋限制模型计算M=1的氧分子体系输入文件
需要注意的是,上述调用自旋限制模型的方法对于其他计算方法也同样适用,例如,当使用B3LYP泛函时,可以通过写成RB3LYP的形式调用自旋限制模型。但在实际的计算中,对于M=1的体系,Gaussian程序的默认选项就是调用自旋限制模型,也就是说即便写成B3LYP的形式,程序也会自动调用自旋限制模型。
1.2 使用自旋非限制模型
第一步:利用GaussView构建氧分子结构。
第二步:编辑输入文件。
利用自旋非限制模型计算M=1的氧分子体系输入文件:

图4.自旋非限制模型计算M=1的氧分子体系输入文件
需要注意的是,对于M=1的体系,若想调用自旋非限制模型进行计算,必须在方法(在这个例子中方法是apfd)前面加上U,也就是写成Uapfd的形式。
2.计算自旋多重度M=3的氧分子体系
2.1 使用自旋非限制模型
第一步:利用GaussView构建氧分子结构。
第二步:编辑输入文件。
利用自旋非限制模型计算M=3的氧分子体系输入文件:
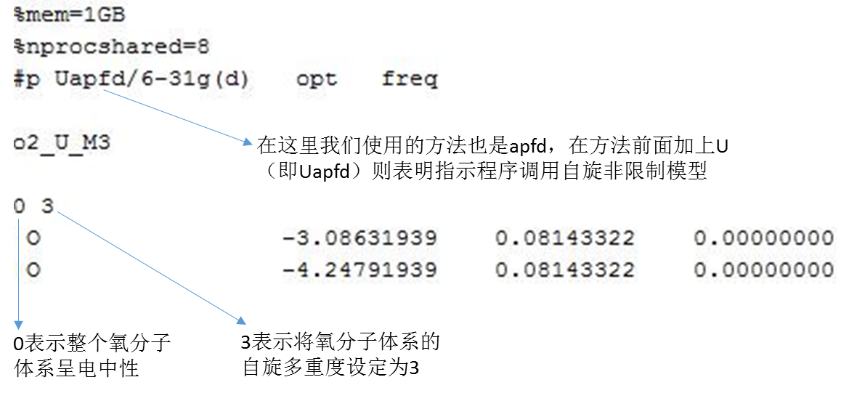
图5. 自旋非限制模型计算M=3的氧分子体系输入文件
需要注意的是,对于M≠1的体系(在这里M=3),Gaussian程序的默认选项就是调用自旋非限制模型,也就是说,在这个例子中,我们也可以写成apfd的形式,程序也会自动调用自旋非限制模型进行计算。
三. 结果分析
我们比较了三种情况下氧分子体系的电子能,发现当M=3时,氧分子的电子能量最低,这也意味着氧分子的基态为三重态,与文献报道相一致。
Table 1. 氧分子体系的电子能
| 计算体系 | M=1 自旋限制模型 | M=1 自旋非限制模型 | M=3 自旋非限制模型 |
|---|---|---|---|
| 能量(Hatree) | -150.141521 | -150.141521 | -150.2070579 |
这些结果也提示我们,面对一个未知的体系时,应该考虑基态分子有可能处于哪些自旋多重度,以便得到合理的结果。
四. 使用GaussView生成输入文件
- 绘制氧分子,设定作业类型
- 设定DFT计算的方法、基组与自旋限制模型
- 设定电荷与自旋多态性
- 预览与提交作业
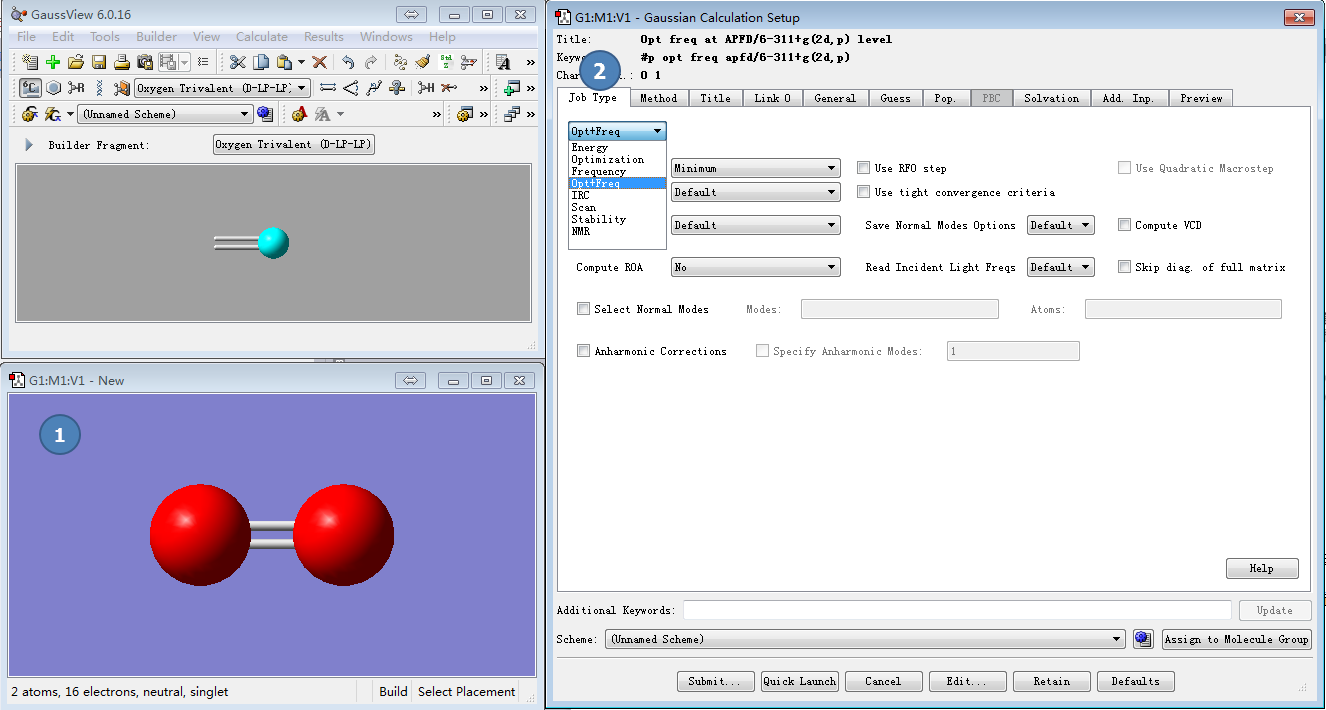
图1. 在3D绘图区绘制氧分子(1),在Job type选项卡里设定作业类型为Opt+freq(2)
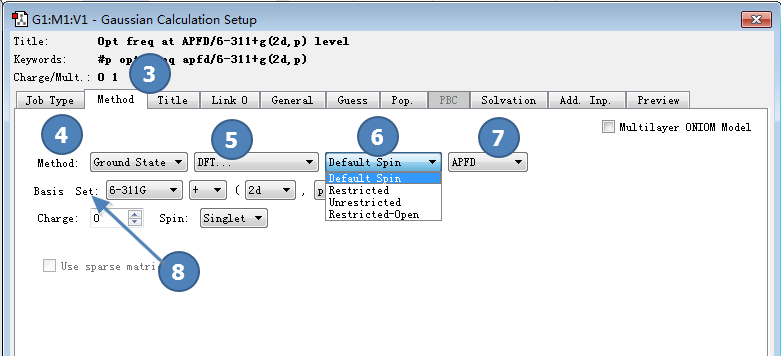
图2. 在Method选项卡(4)里设定基组与方法(5、7、8)以及自旋限制模型(6)
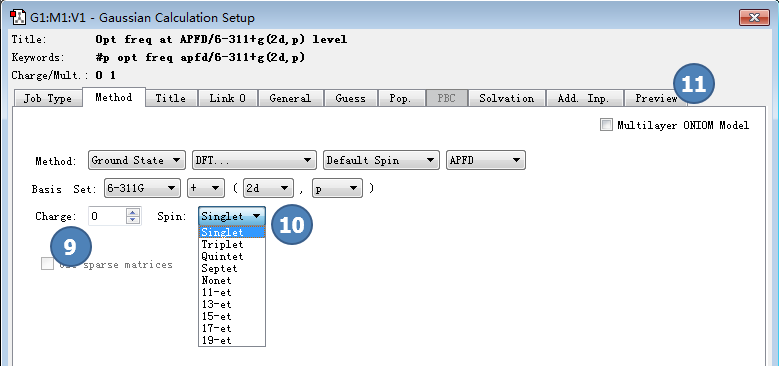
图3. 设定电荷(9)与自旋多态性(10)
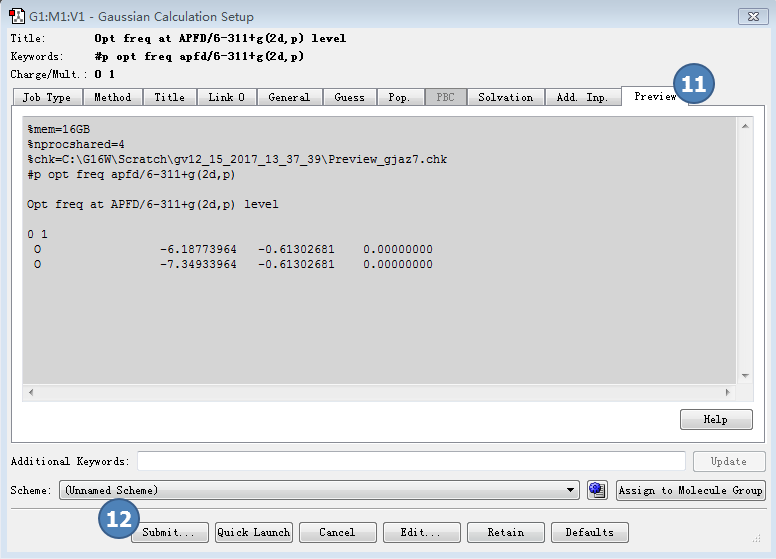
图4.预览(11)与提交作业(12)
五. 参考资料
- Exploring Chemistry with Electronic Structure Methods, 3rd ed., Gaussian, Inc.: Wallingford, CT, 2015. J. B. Foresman and Æ Frisch



