摘要:为了发现全新的p38 MAPK抑制剂,Timothy和同事们使用FieldScreen这一基于配体的虚拟筛选技术,对120万个可购买化合物进行筛选。根据与已知配体的分子场相似性,从中挑选了58个不同于已报道的p38抑制剂骨架的化合物进行生物学分析。其中,11个化合物在10 μM浓度下表现出≥ 20%的抑制率。然后,通过购买或合成方式对其中两个骨架进行衍生化,获得了一个潜在先导化合物(pIC50 = 6.4)。最后,使用FieldAlign工具对这些衍生物进行叠合,以研究他们的SAR。
Timothy J. Cheeseright, et al. Novel Lead Structures for p38 MAP Kinase via FieldScreen Virtual Screening. J. Med. Chem. 2009, 52, 4200–4209.
摘要
p38 MAPK一直以来都得到制药工业的青睐,至今仍是治疗炎症的有效而引人注目的靶点。为了发现全新的p38抑制剂,Timothy和同事们使用FieldScreen这一基于配体的虚拟筛选技术,对120万个可购买化合物进行筛选。根据与已知配体的分子场相似性,从中挑选了58个不同于已报道的p38抑制剂骨架的化合物进行生物学分析。其中,11个化合物在10 μM浓度下表现出 ≥ 20%的抑制率。然后,通过购买或合成方式对其中两个骨架进行衍生化,获得了一个潜在先导化合物(pIC50 = 6.4)。最后,使用FieldAlign工具对这些衍生物进行叠合,以研究它们的SAR。
操作流程
1. 准备参比分子
从蛋白-配体复合物晶体结构 1m7q、1yw2和1ouk中分别抽取配体分子。分析配体分子的结合模式及电性分布,对配体分子的结构进行裁剪(图1)。
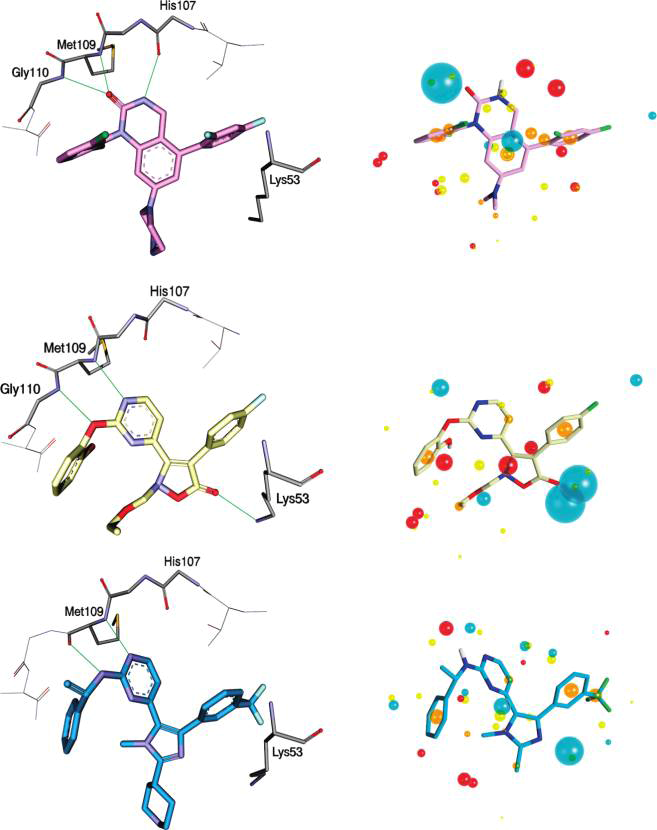
Figure 1. 用作FieldScreen虚拟筛选的搜索参照分子在蛋白-配体复合物晶体结构中的结合模式及其场点模式(Field point pattern):分别来自PDB编号1m7q(上)、1yw2(中)和1ouk(下),场地标记为蓝色=负电,红色=正电,橙色=疏水,黄色=表面。
2.虚拟筛选
分别以三个配体分子作为搜索参照结构,使用FieldScreen对商业库进行虚拟筛选,分别获得250个结果,合并去重并去掉与已报道的p38抑制剂同一骨架的化合物后,得到746个化合物(图2)。
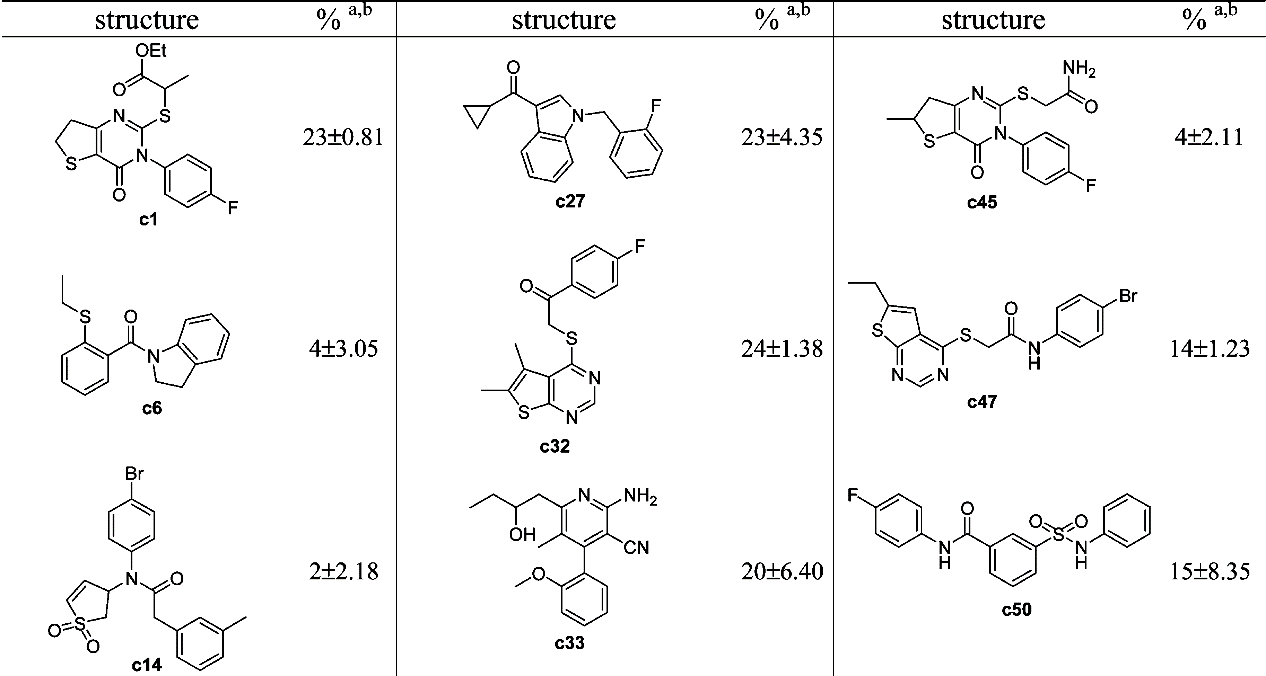
Figure 2. 虚拟筛选部分结果及其生物活性测试结果
3.聚类分析与化合物挑选
采用基于2D拓扑结构进行聚类分析,得到96类和311个单体化合物。通过2D观察和对原来搜索参照结构的3D叠合,挑选出58个化合物用作生物学验证。
4.生物学验证
以ATF-2为底物,ATP作为辅因子进行酶实验,结果分析表明,11个化合物(命中率19%)在10 μM浓度下表现出≥ 20%的抑制率。
4. SAR研究
4.1 专利文献调研,确定先导化合物骨架
在专利文献调研及生物活性测试结果的基础上,确定了由苗头化合物向先导化合物研究有2类骨架,分别是噻二唑类化合物c15和吡喃吡唑类化合物c38。
4.2 骨架衍生
基于两个骨架化合物进行衍生化,通过购买或者合成的方式获得衍生物,然后进行生物活性测试。测试结果表明,20个c38类似物仅具有中等SAR,32个c15类似物IC50可达0.44μM。
4.3 理解SAR
通过FieldAlign将c15的类似物叠合到原来的搜索参照结构上,分析结果与观察到的SAR十分一致,很好地解析了c15类似物的SAR(图3)。
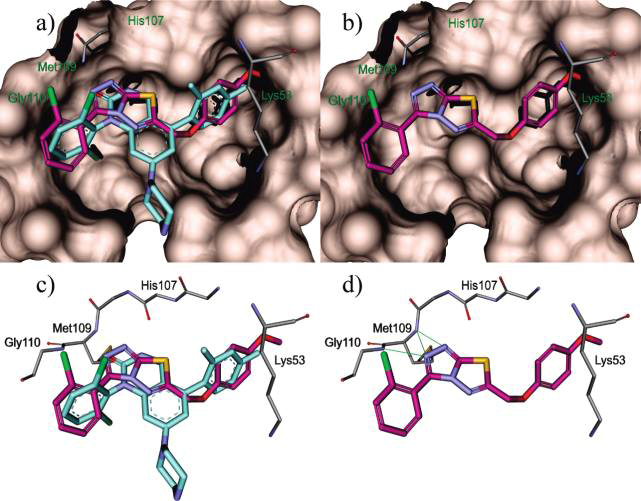
Figure 3. 将叠合后的结构放在结合口袋里展示其相互作用模式。
结论
使用FieldScreen能够极大地提高全新骨架抑制剂的虚拟筛选命中率,能够有效绕开专利保护,从而建立自己的知识产权。通过FieldAlign对衍生物进行基于场的3D分子叠合,获得与观察相一致的结果,能够很好地理解SAR。
亮点
- 对比蛋白-配体复合物晶体结构中的配体结合模式与Cresset产生的场点模式,对参照分子进行适当的结构裁剪,提高了模拟的准确性;
- 采用多个参照分子叠合能更好地描述配体的结合要求,获得与观察一致的结果。
关键软件与技术
Cresset的FieldScreen和FieldAlign技术。FieldScreen是Cresset公司的重要技术之一,实现在Blaze中;FieldAglin是一个分子叠合的程序,是Forge的一部分。



