摘要:电子密度差图常用于激发态跃迁的结果分析, 然而有时电子密度差图并不能清楚、确切给出结果,此时,自然跃迁轨道(Natural transition orbitals, NTOs)可能就能帮上忙。本教程演示了如何进行NTOs计算:激发态计算,确定NTO分析的激发态,NTOs计算。
原文:http://www.gaussian.com/g_blog/faq4.htm
改编:肖高铿
一. 自然跃迁轨道简介
Gaussian的TD-DFT方法为激发态的研究提供了非常实用的方法,因为它的结果与DFT计算研究基态一样精确。电子密度差图常用于激发态跃迁的结果分析(见教程:Gaussian教程–GaussView绘制电子密度差图)。然而有时电子密度差图并不能清楚、确切给出结果,此时,另一种技术–自然跃迁轨道(Natural transition orbitals, NTOs)可能就能帮上忙。
NTOs是一种定性描述电子激发便利的方法,从TD能量计算的跃迁密度开始可以非常快速地计算获得NTOs。NTOs将经典的轨道转化为紧凑的形式,将每个激发态跃迁用一对或两对的轨道表示:NTOs跃迁从激发的占据轨道(occupied transtion orbitals,也称为hole)跃迁到非占据跃迁轨道(unoccupied transtion orbitals,也称为particle或electron)。当一个激发态不存在单个优势轨道跃迁,需要用很多轨道系数相近的经典轨道跃迁来描述的时候,此时若电子密度差不能清楚归属跃迁性质,NTOs经常可以帮上大忙。更详细的NTOs介绍,参见文献[Martin03]。
二. 如何计算NTOs
三步完成NTOs计算:
- TD-DFT计算激发态,保存checkpoint文件
- 检查计算结果,确认需要分析的激发态
- 单点计算生成感兴趣激发态的NTOs
对于不同激发态的NTOs:重复计算第三步。
三. 操作步骤
1.激发态计算
第一步激发态计算例子如下。这是一个TD-DFT计算,在这之前已经被优化并确认是一个极小点结构。
1 2 3 4 5 6 | %Chk=tddft # B3LYP/6-311+G(d,p) TD(NStates=40) TD-DFT excited state calculation: B3LYP/6-311+G(2d,p) !此处省略了molecule specification部分 |
2. 确认需要分析的激发态
假设,我们对第3激发态感兴趣,并对该激发态进行NTOs分析。
3. NTOs生成与可视化分析
现在,我们需要进行计算以生成NTOs并提供给GaussView进行可视化分析。
在本例中,我们需要计算第三激发态的NTOs:
1 2 3 | %OldChk=tddft %Chk=state3 # B3LYP/6-311+G(2d,p) Geom=AllCheck Guess=(Read,Only) Density=(Check,Transition=3) Pop=(Minimal,NTO,SaveNTO) |
Pop=NTO选项告诉Gaussian进行NTO计算,Pop=SaveNTO选项告诉Gaussian将Checkpoint文件中基态的轨道替换为计算获得的NTOs。GaussView可以用于展示checkpoint文件中的任意轨道,包括NTOs,所以使用GaussView的时候无需做任何特殊修改或设置。
如果想生成第6激发态的NTOs,可以在上面的输入文件里通过Link1加入该作业:
1 2 3 4 | --Link1-- %OldChk=tddft %Chk=state6 # B3LYP/6-311+G(2d,p) Geom=AllCheck Guess=(Read,Only) Density=(Check,Transition=6) Pop=(Minimal,NTO,SaveNTO) |
四. 举例
1. Pt(dcbpy)Cl2的激发态计算
Pt(dcbpy)Cl2结构如图1所示:
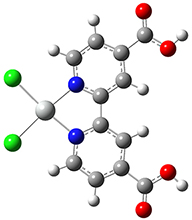
图1.Pt(dcbpy)Cl2的结构
计算细节(见Roy09):
route部分:TD(NStates=40) CAM-B3LYP/Gen Pseudo=Read
基组(ECPs): Pt用LANL08,其它原子用6-311G(d)
TD-DFT计算获得第19激发态结果如下:
1 2 3 4 5 6 7 8 9 | Excited State 19: Singlet-A 4.7936 eV 258.64 nm f=0.0002 … 78 -> 90 0.41835 78 -> 92 -0.18686 78 -> 95 0.17948 79 -> 91 0.42043 79 -> 94 -0.10009 79 -> 99 0.12527 80 -> 90 0.15807 87 -> 92 0.11388 |
根据该激发态跃迁的各个轨道系数, 没有一个跃迁占绝对优势。下图2展示了分子轨道及其跃迁,并标注上了对应的系数:
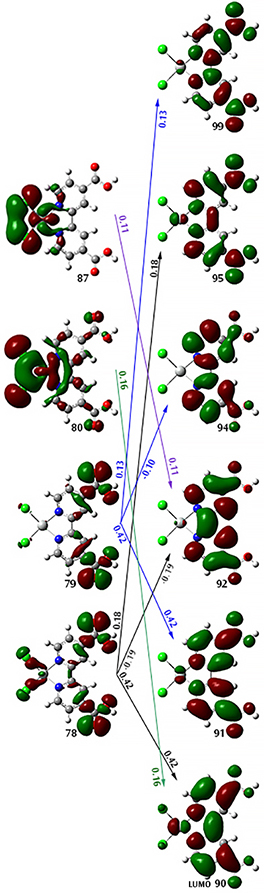
图2.Pt(dcbpy)Cl2的分子轨道与跃迁
但是对该激发态进行NTOs计算,获得两对NTOs(如图3、4所示),可以极大地简化了跃迁过程的表征:
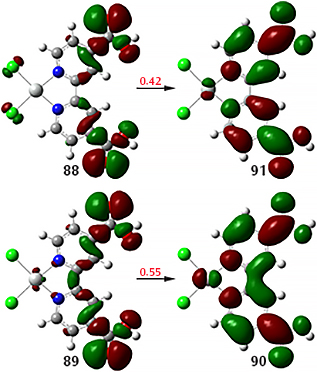
图3.Pt(dcbpy)Cl2的两对NTOs
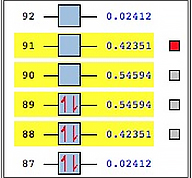
图4. Pt(dcbpy)Cl2的两对NTOs
五. 文献
[Martin03] Martin, R. L. “Natural transition orbitals.” JCP 2003, 118, 4775-4777. doi:10.1063/1.1558471
[Roy09] Roy, L. E.; Scalmani, G.; Kobayashi, R.; Batista, E. R.“Theoretical studies on the stability of molecular platinum catalysts for hydrogen production.” Dalton Trans. 2009, 6719–6721. doi:10.1039/b911019b



